Newsletter Spectra Diagnostic N°44

INFORMATIQUE DE LABORATOIRE
Logiciel de validation biologique : nouvelle version plus flexible
Valab®, pionnier dans l’automatisation de la validation biologique et avec plus de 770 000 dossiers expertisés par jour au niveau national et international, lance sa nouvelle version majeure, V16.
Valab® V16 est une évolution en profondeur, pensée pour répondre aux besoins de ses utilisateurs et aux exigences croissantes en matière de sécurité.
Des évolutions dans l’expertise biologique :
• De nouvelles analyses « clé en main » modélisées dans les spécialités de biochimie, d’oligo-éléments, de gaz du sang et de bactériologie.
• L’ajout de nouveaux renseignements cliniques et thérapeutiques dans plusieurs catégories : maladie, traitements, chirurgie, symptômes, FIV/PMA, etc.
• Des avancées dans les mécanismes de règles d’expertise.
De nouvelles fonctionnalités pour la gestion et l’exploitation des données :
• Compatibilité des dossiers tests dans le contrôle continu
• Export des données statistiques au format CSV
Des renforcements en matière de sécurité :
• Intégration d’un annuaire LDAP
• Prise en compte continue des exigences RGPD et de la protection des données sensibles
• Blocage et traçage des tentatives multiples de connexion frauduleuse
Des nouveautés pour l’international :
• Ajout de la langue portugaise au logiciel
• Traduction de l’interface du logiciel et des documents de qualité en allemand, anglais, espagnol et portugais.
Des ergonomies repensées pour une navigation plus fluide, au sein de différentes fenêtres du menu Simulation, du module Auto-Expert, du paramétrage des analyses et des tables de correspondance (filtrage, tri, recherche).
Cette nouvelle version est conçue pour aborder tout type de laboratoire au-delà de la biologie médicale de routine. Une version
« sans analyses préchargées » permet de construire et d’exploiter une
application « sur mesure » dans le domaine souhaité, avec la possibilité d’utiliser les analyses « clé en main » du catalogue de la société.
ALZHEIMER
Maladie d’Alzheimer : calculer le ratio Aβ42/Aβ40
Le diagnostic de la Maladie d’Alzheimer s’apprête à connaître une évolution majeure. Roche Diagnostics souhaite accompagner cette mutation avec le développement de son portefeuille de tests diagnostiques LCS (liquide cérébrospinal) et sanguins. La société lance le test Elecsys β-Amyloid (1-40) CSF qui, combiné au test Elecsys β-Amyloid (1-42) CSF, permet d’établir le ratio Aβ42/Aβ40. Ce ratio aide à l’évaluation de la pathologie amyloïde chez les sujets adultes présentant des troubles cognitifs et faisant l’objet d’une évaluation pour la maladie d’Alzheimer ou d’autres causes de troubles cognitifs.
Ainsi, Roche propose désormais pour le diagnostic de cette maladie un menu sur le LCS complet et approuvé conformément à la réglementation relative aux dispositifs médicaux de diagnostic in vitro, sur les systèmes cobas e.
Côté plasmatique, après la sortie récente du test Elecsys Phospho-Tau (181P) Plasma, de nouveaux tests sanguins seront lancés par la société en 2026.
IMMUNO-ANALYSE
Différencier bactéries et virus en environ 20 minutes
Beckman Coulter Diagnostics, société du groupe Danaher, a obtenu le marquage CE IVDR pour le test Access MeMed BV. Cette certification permet une large disponibilité d’un test à haut débit basé sur la réponse de l’hôte, qui aide les cliniciens à différencier les infections bactériennes des infections virales en environ 20 minutes. Il intègre la mesure de trois protéines clés de la réponse immunitaire de l’hôte (TRAIL, IP-10 et CRP) dans un score indiquant la probabilité d’une infection bactérienne ou virale. Ce test a démontré une valeur prédictive négative pouvant atteindre 99 % pour aider à exclure une infection bactérienne.
Validé pour une utilisation sur la base installée des automates d’immunoanalyse DxI 9000 et Access 2 de Beckman Coulter, ce test permet une différenciation rapide et fiable des infections, tout en s’intégrant aux infrastructures et aux flux de travail existants des laboratoires. La société a collaboré avec MeMed, leader des technologies avancées d’analyse de la réponse de l’hôte, afin d’intégrer le test éprouvé MeMed BV® dans les laboratoires centraux. Ce test a démontré sa capacité à améliorer la prise de décision clinique, à permettre aux médecins de réduire l’usage inutile des antibiotiques et à soutenir les initiatives de bon usage des antimicrobiens.
Des études récentes menées en conditions réelles auprès de près de 6 000 patients adultes et pédiatriques ont montré que les cliniciens hésitent quant à la prescription d’antibiotiques dans environ 16 à 29 % des cas. Après réception des résultats MeMed BV, les médecins ont indiqué que le test avait soutenu ou modifié la prise de décision clinique dans environ 82 à 87 % des cas.
BIOLOGIE MOLECULAIRE
Diagnostic POC des infections respiratoires et pharyngées

bioMérieux a vu ses deux tests Biofire® Spotfire® Respiratory/Sore Throat plus (R/STplus) Panel et Biofire® Spotfire® Respiratory/Sore Throat plus (R/STplus) obtenir le marquage CE selon l’IVDR. Cette certification inclut la classification « Near-Patient Testing » autorisant une utilisation au chevet du patient. Ces tests multiplex PCR peuvent détecter simultanément les agents pathogènes les plus souvent responsables d’infections respiratoires et de maux de gorge, dans un délai compatible avec la durée d’une consultation médicale classique.
Dans un contexte où de multiples pathogènes respiratoires circulent simultanément, l’identification rapide et précise de l’agent responsable permet de mettre en place dans les meilleurs délais une prise en charge adaptée et contribue notamment à un usage efficient des antibiotiques.
Ces deux tests, compatibles avec l’instrument compact Biofire® Spotfire®, sont capables d’identifier simultanément, en 15 minutes environ, les acides nucléiques des bactéries, virus et sous-types viraux les plus fréquemment responsables d’infections respiratoires ou pharyngées.
La version Panel Mini et la version Panel détectent respectivement 6 à 15 agents pathogènes, incluant notamment le rhinovirus/entérovirus humain, le streptocoque A, les virus de la grippe A/B, le virus respiratoire syncitial (VRS) et le SARS-CoV-2. Ensemble, ces deux panels offrent une solution flexible et sur-mesure, permettant aux cliniciens de sélectionner d’emblée le test le plus adapté au profil de chaque patient.
Le test Biofire® Spotfire® R/STplus Panel, vient remplacer la version Biofire® Spotfire® R/ST Panel commercialisée jusque-là avec le marquage CE selon la directive IVDD.
Les échantillons peuvent être prélevés à l’aide d’un écouvillon nasopharyngé ou oropharyngé, en fonction du type d’infection suspecté. La version Panel Mini offre également une troisième méthode de prélèvement, par écouvillonnage nasal antérieur, spécifiquement compatible avec le menu respiratoire.
Ces deux nouveaux tests seront disponibles au deuxième trimestre 2026 dans les pays reconnaissant le marquage CE. Ils seront ensuite déployés dans d’autres pays, hors États-Unis, en tenant compte des réglementations locales.
IMMUNO-CHROMATOGRAPHIE
Diagnostic rapide en antibiorésistance amélioré

La résistance aux antibiotiques constitue aujourd’hui l’une des plus graves menaces pour la santé mondiale. Elle compromet la prévention et le traitement efficace d’un nombre croissant d’infections bactériennes. L’antibiorésistance entraîne une prolongation des hospitalisations, une hausse de la mortalité et une augmentation des dépenses médicales.
Face à cet enjeu sanitaire majeur, chaque avancée technologique représente une opportunité déterminante pour mieux détecter, prévenir et contrôler l’antibiorésistance.
C’est dans cette perspective que le fabricant Coris BioConcept a amélioré son kit Resist 5, test de diagnostic rapide in vitro permettant la détection des carbapénémases OXA 48, KPC, NDM, VIM et IMP dans les cultures bactériennes.
Distribué par Launch Diagnostics France dès cet été en IVDR, ce nouveau test proposera une cassette optimisée : une seule zone de dépôt pour deux bandelettes de migration, un signal amplifié pour un meilleur confort de lecture et une capacité étendue à 8 marqueurs, en plus des deux contrôles intégrés.
La gamme Resist regroupe en outre des tests rapides couvrant un large panel de paramètres (OXA 48, KPC, NDM, VIM, IMP, CTX M, OXA 23, OXA 40(24), OXA 58, OXA 163). Présentant des performances équivalentes à celles des méthodes moléculaires, ces tests peuvent être réalisés à partir de différents types d’échantillons — culture bactérienne, hémoculture, écouvillon rectal — avec des résultats disponibles en moins de 15 minutes.
Cette gamme comprend également une offre étendue de contrôles de qualité dédiés aux tests rapides d’antibiorésistance (OXA 48, KPC, NDM, VIM, IMP, CTX M15, CTX M14, OXA 23, OXA 40(24), OXA 58, OXA 163).
Société pionnière du diagnostic rapide en antibiorésistance depuis 1996, Coris BioConcept s’appuie sur une solide expertise industrielle et scientifique. Ces produits sont fabriqués intégralement en Belgique et distribués dans le monde entier.

Roche inaugure une usine d’IA NVidia pour accélérer sa R&D
Roche annonce l’expansion de son infrastructure mondiale d’IA avec le déploiement d’une « usine d’IA » à grande échelle reposant sur une pile complète de technologies de calcul et d’IA accélérées NVIDIA. L’installation comprend 2 176 GPU haute performance déployés sur site aux États-Unis et en Europe et intégrés à l’ensemble de la chaîne de valeur. Avec cet investissement, la capacité combinée sur site et dans le cloud dépasse désormais 3 500 GPU Blackwell, une puissance que Roche présente comme la plus importante annoncée dans l’industrie pharmaceutique.
Cette expansion marque une nouvelle étape de la collaboration stratégique engagée avec NVIDIA en 2023 pour accélérer le développement de diagnostics et de thérapies grâce à des données de haute qualité et à l’IA. « Dans le secteur de la santé, le temps est un facteur crucial », souligne Wafaa Mamilli, directrice du numérique et de la technologie chez Roche, mettant en avant une plateforme conçue pour intégrer l’IA de la découverte à la fabrication et jusqu’à la commercialisation.
La plateforme, présentée comme un système de supercalcul haute performance, soutient plusieurs usages. En R&D, NVIDIA BioNeMo alimente le modèle « Lab-in-the-Loop » de Roche, qui relie les expériences de biologie et de chimie à des modèles d’IA afin de tester des hypothèses à grande échelle et d’accélérer les découvertes. Dans l’industrie, des jumeaux numériques fondés sur NVIDIA Omniverse aident à optimiser procédés et conception d’usines. Pour le diagnostic, NVIDIA Parabricks vise à extraire plus rapidement des informations exploitables à partir de grands ensembles de données ; en pathologie numérique, l’analyse d’images doit permettre de détecter des schémas subtils. En santé numérique, Roche s’appuie sur NVIDIA NeMo Guardrails pour encadrer une IA conversationnelle de qualité médicale.
Cette plateforme doit ainsi consolider la position de Roche dans la découverte et le développement de médicaments pilotés par l’IA, comme l’a expliqué Aviv Regev (Genentech, gRED), évoquant des modèles prédictifs plus sophistiqués et une accélération de la transformation des connaissances biologiques en médicaments vitaux.
Pour Roche, cette « usine d’IA » s’inscrit dans une transformation numérique globale : l’IA est conçue pour enrichir l’expertise humaine et élargir l’accès aux capacités de supercalcul à l’échelle de l’organisation. L’objectif affiché est d’aider les équipes, partout dans le monde, à relever des défis complexes liés aux maladies humaines et à accélérer la prévention, l’enrayement des maladies et la guérison.
Sysmex regroupe ses trois sièges européens sur un nouveau campus à Hambourg

Sysmex a officiellement ouvert son nouveau campus à Hambourg-Alsterdorf, achevant ainsi la relocalisation de son siège EMEA de Norderstedt vers la ville. Environ 780 employés du siège européen, de la filiale allemande et de la recherche et du développement travaillent désormais ensemble sur le nouveau site, renforçant ainsi la position de Hambourg en tant que site clé pour les sciences de la vie et la technologie médicale.
Avec cette ouverture, Sysmex réunit pour la première fois sous un même toit trois entités européennes clés : Sysmex Europe SE, Sysmex Deutschland GmbH et Sysmex R&D Center Europe GmbH. Le campus couvre environ 12 300 mètres carrés d’espace locatif et marque une étape importante dans la stratégie de croissance à long terme de l’entreprise dans la région EMEA.
« Aujourd’hui marque le début d’un nouveau chapitre pour Sysmex en Europe », a déclaré Alain Baverel, PDG de Sysmex Europe SE. « Avec ce campus, nous avons créé un environnement qui rapproche les gens, la recherche et la technologie. Il renforce notre position dans la région EMEA et crée les conditions propices aux innovations qui façonneront l’avenir du diagnostic en laboratoire. »
En choisissant Hambourg-Alsterdorf, Sysmex se positionne à proximité de grandes institutions de recherche et d’un solide écosystème des sciences de la vie. L’entreprise a évoqué la disponibilité de professionnels qualifiés, l’excellente infrastructure et la position centrale de Hambourg en Europe comme des facteurs décisifs pour son déménagement.
Le campus établit de nouvelles normes en termes de durabilité et de conception moderne du lieu de travail. Situé entre l’aéroport et l’hôpital universitaire, et à proximité de l’Alster, le bâtiment a reçu la première certification LEED (Leadership in Energy and Environmental Design), soulignant l’engagement de Sysmex en matière de responsabilité environnementale et de construction durable. Des façades vertes en clinker, des toits verts accessibles et un concept énergétique intelligent permettent aux bâtiments de répondre aux normes élevées de l’UE.
À l’intérieur, des concepts spatiaux flexibles basés sur le principe du travail par activité permettent aux employés de choisir leur espace de travail en fonction de leur tâche, qu’il s’agisse de zones de concentration et de collaboration calmes, d’environnements de laboratoire hautement spécialisés ou de centres de formation.
PROFESSION
G7 One Health Summit : un pacte mondial pour l’accès aux diagnostics
Le 7 avril 2026, une coalition de plus de 20 partenaires internationaux a annoncé le Pacte mondial pour l’accès aux diagnostics (Global One Health Diagnostic Access Compact) lors du Sommet du G7 One Health à Lyon (France). Cette nouvelle initiative sert de catalyseur pour les leaders internationaux de différents secteurs pour accélérer l’accès aux diagnostics, permettre une détection plus précoce et une meilleure surveillance des pathogènes, et améliorer la réponse aux menaces existantes et émergentes en santé humaine, animale et environnementale. En alignant les efforts, les partenaires entendent renforcer la préparation mondiale grâce à des approches « One Health » fondées sur la science.
Partout dans le monde, les autorités sanitaires peinent à suivre le rythme de menaces de plus en plus interdépendantes — qu’il s’agisse du changement climatique qui favorise la propagation des espèces vectrices de maladies, de la multiplication des cas de transmission des maladies de l’animal à l’homme, ou encore de l’aggravation de la résistance aux antimicrobiens. Dans de nombreuses régions, les capacités élémentaires à identifier des bactéries et autres agents pathogènes sont rares voire inexistantes, les informations relatives à la santé humaine, animale et environnementale restent cloisonnées et ralentissent la détection. Il en résulte des retards de diagnostic, des traitements inappropriés, une utilisation inutile d’antibiotiques, une détérioration des résultats pour les patients et une détection trop lente des nouveaux agents pathogènes et des épidémies.
Alors que les pays affinent leurs stratégies de lutte contre la résistance aux antimicrobiens et préparent leurs prochains engagements dans le cadre du G7 et des instances multilatérales, il est urgent de mener des actions concrètes et concertées. C’est dans ce contexte que ces partenaires ont élaboré ce Pacte mondial — une initiative collective visant à combler les lacunes en matière de diagnostic, à harmoniser les actions entre les différents secteurs et à aider les pays dans la construction de systèmes de santé plus résilients et fondés sur les données.
Ce Pacte marque une étape cruciale : en s’alignant sur les cadres politiques nationaux et internationaux et en plaidant pour une collaboration public-privé accrue, il vise à améliorer la précision des traitements et les stratégies de prévention, à renforcer les systèmes de santé et à faire face à la menace croissante de la résistance aux antimicrobiens et d’autres menaces existantes et émergentes.
Partenaires et engagements du Pacte
Ce Pacte est porté par un groupe de partenaires comprenant des acteurs de la société civile, des acteurs privés, des sociétés professionnelles et scientifiques, des fondations et des initiatives de santé mondiale engagés dans l’action One Health et la gestion de la résistance aux antimicrobiens. Ensemble, ils représentent des dizaines de milliers de professionnels spécialistes des maladies infectieuses et de la microbiologie et contribuent au diagnostic, à la prévention et au traitement couvrant les parcours de soin de dizaines voire de centaines de millions de patients chaque année au sein des systèmes de santé de plus de 130 pays.
En adoptant ce Pacte, les signataires s’engagent collectivement à faire avancer quatre axes prioritaires :
1. Améliorer l’accès à des outils de diagnostic adaptés et de haute qualité pour tous. Élargir l’accès abordable aux diagnostics prioritaires à tous les niveaux de soins et dans toutes les régions géographiques ; favoriser le partage de données et de connaissances pour éclairer les décisions de santé publique.
2. Renforcer la gestion responsable et l’utilisation appropriée des diagnostics et des antibiotiques. Lier l’accès aux antibiotiques de dernière ligne à une utilisation accrue des outils diagnostiques ; intégrer des algorithmes de diagnostic et une formation en bonne gestion des antibiotiques adaptée au contexte.
3. Investir en R&D pour répondre aux besoins de santé publique. Faire progresser l’innovation en matière de diagnostics humains, vétérinaires et environnementaux, en incluant des solutions adaptées aux contextes des pays à ressources limitées, grâce à des partenariats public-privé et des collaborations ouvertes à l’échelle de l’industrie, du milieu universitaire, des ONG et des partenaires publics.
4. Améliorer la valorisation et l’intégration des diagnostics. Travailler avec les gouvernements, les payeurs et les partenaires mondiaux pour garantir que les diagnostics soient correctement valorisés, remboursés et intégrés dans les parcours cliniques et de santé publique, ainsi que dans les milieux de santé animale, reflétant ainsi des bénéfices en aval tels que la réduction de la consommation d’antimicrobiens et des réductions de coûts.
Prochaines étapes du Pacte
Les signataires du Pacte mondial pour l’accès au diagnostic s’engagent à faire progresser cette initiative commune, tout en reconnaissant que les contributions spécifiques varieront selon les missions individuelles, les modèles économiques et les domaines d’activité. Lorsque cela est approprié, les organisations collaboreront avec les gouvernements nationaux et les organisations multilatérales, y compris le G7, pour soutenir les progrès et contribuer à garantir que les diagnostics et la surveillance soient plus systématiquement pris en compte dans les engagements politiques, les mécanismes de financement et les stratégies de santé mondiale.
Liste complète des partenaires : African Society for Laboratory Medicine, American Society for Microbiology, AMR Action Fund, Bavarian Nordic, bioMérieux, British Society for Antimicrobial Chemotherapy, CARB-X, Ceva Animal Health, Copan Group , Danaher Corporation, DxAMR Collaborative, European Society of Clinical Microbiology and Infectious Diseases, Infectious Diseases Society of America, InnotiveDx, International Society of Antimicrobial Chemotherapy, LifeArc, Liofilchem, Nostics, Novo Nordisk Foundation, Roche Diagnostics, Sysmex, Waters Corporation
France 2030 : Montpellier va expérimenter l’hôpital augmenté
Le 9 avril, à l’occasion du Tour de France de l’innovation en santé à Nantes, consacrée aux données de santé, biobanques et cohortes comme leviers d’innovation, Stéphanie Rist, ministre de la Santé, des familles, de l’autonomie et des personnes handicapées, aux côtés du Secrétariat général pour l’investissement (SGPI), en charge de France 2030, et de l’Agence de l’innovation en santé (AIS), ont annoncé le financement du premier projet d’envergure d’hôpital augmenté par l’IA, souverain et réplicable : Alliance Santé IA.
Un événement de lancement officiel est prévu le 16 juin prochain à Montpellier afin de présenter en détail ce projet et le rôle de chacun des membres du consortium mené par le CHU de Montpellier et ADLIN Science.
Depuis plusieurs années, l’État a fait de l’IA une priorité stratégique, avec l’ambition de disposer d’une offre d’IA souveraine, notamment au travers des investissements conséquents du plan France 2030 et d’une stratégie IA pilotée en interministériel. Décliné dans le domaine de la santé, cet engagement vise à améliorer les diagnostics et les parcours de soins, soutenir l’innovation en recherche médicale, encourager l’appropriation des outils d’IA par les professionnels et garantir un cadre éthique, sécurisé et responsable autour de l’utilisation des données de santé.
Au total, tous programmes confondus (recherche ou soutien aux entreprises), le montant d’investissements dans des projets centrés sur l’IA en santé s’élève à environ 400 M€ depuis le lancement des programmes d’investissements d’avenir et désormais du plan Innovation santé France 2030, volet santé de France 2030.
Une expérimentation d’ampleur
Dans ce cadre, la ministre annonce un financement de 14,9 millions d’euros de France 2030 pour le projet Alliance Santé IA.
Co-construit par le CHU de Montpellier et ADLIN Science, le projet est porté par un consortium d’acteurs de référence réunissant le CINES, l’Inria, ANA Healthcare et Numalis, avec un partenariat structurant avec l’hébergeur français Scaleway.
Ce projet a pour ambition de créer le premier hôpital pilote augmenté par l’IA, basé sur une infrastructure souveraine, évolutive et réplicable. Cette initiative constitue un démonstrateur permettant de lever des verrous structurels majeurs dans le domaine de la santé, grâce à l’évaluation des impacts en conditions réelles, en vue d’une généralisation à d’autres établissements de santé.
Programmes d’investissements d’avenir France 2030
RICAI : 3 Bourses de Microbiologie et/ou de Maladies Infectieuses
En 2026, l’Association de Chimiothérapie Anti-Infectieuse (ACAI) propose un total de 3 bourses (Microbiologie, Maladies Infectieuses, Soutien au développement) adressées respectivement à la SFM et la SPILF pour favoriser la mobilité de jeunes praticiens ou chercheurs. Les demandes seront évaluées par au moins 3 relecteurs du Comité Scientifique de la RICAI.
Il s’agit de 3 bourses dédiées à une activité de recherche clinique ou fondamentale dans tous les domaines de la Microbiologie (bactériologie, virologie, parasitologie, mycologie, hygiène hospitalière) et/ou des Maladies infectieuses (chimiothérapie anti-infectieuse, pathogénie, épidémiologie…).
Les candidats, âgés de moins de 40 ans, devront être titulaires d’un Master 2 validé, réaliser une mobilité de 12 à 24 mois, et disposer d’un co-financement pour la réalisation de la mobilité.
La date limite de candidature est fixée au 15 septembre 2026 à minuit. La publication et l’annonce des résultats sera réalisée lors de la RICAI 2026.
Alzheimer : de nouvelles cellules impliquées
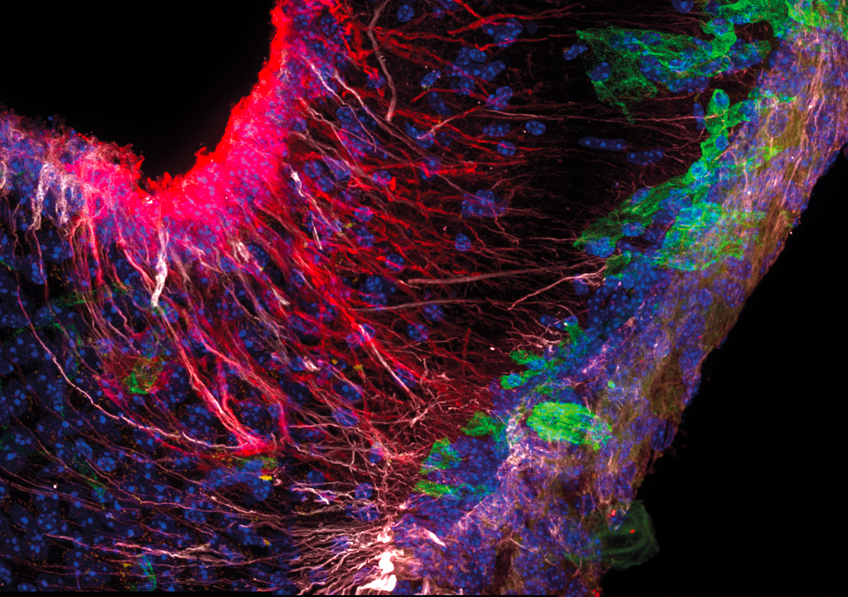
Les tanycytes (en blanc) capturent la protéine Tau (rouge) circulant dans le LCS pour la transporter le long de leurs prolongements/bras qui traversent le tissu cérébral et entrent en contact avec les vaisseaux sanguins (en vert) dans lesquels ils déversent cette protéine impliquée dans la pathologie d’Alzheimer lorsqu’elle s’accumule dans le cerveau. © Vincent Prévot/Inserm
Une étude menée par une équipe Inserm, Université de Lille et CHU de Lille met en lumière un mécanisme jusqu’ici peu exploré dans la maladie d’Alzheimer : le rôle des tanycytes, des cellules situées à l’interface entre le liquide cérébrospinal (LCS) et la circulation sanguine. La maladie se caractérise notamment par l’accumulation anormale de la protéine Tau sous une forme pathologique dans le cerveau. Normalement, Tau, libérée dans le LCR, est ensuite éliminée vers le sang ; lorsque Tau s’agrège dans les neurones, elle perturbe leur fonctionnement, favorise leur dégénérescence et conduit au déclin cognitif. Les mécanismes responsables de cette accumulation restant incomplets, les chercheurs ont cherché à déterminer si les tanycytes, connus pour assurer des échanges essentiels (par exemple le transport de la leptine impliquée dans la satiété), pouvaient participer à l’évacuation de Tau et, en cas de dysfonctionnement, contribuer à la pathologie.
Grâce à des expériences de traçage fluorescent chez l’animal, l’équipe a d’abord montré que Tau injectée dans le LCS est captée par les tanycytes puis acheminée le long de leurs prolongements jusqu’aux capillaires, suggérant une voie de transfert vers le sang. Cette hypothèse est confirmée en bloquant leur fonctionnement par expression ciblée de toxine botulique : l’évacuation de Tau du LCS vers la circulation est alors fortement réduite, indiquant que les tanycytes constituent une voie majeure d’élimination de Tau hors du cerveau. Chez des souris présentant des niveaux élevés de Tau, l’inhibition des tanycytes accélère l’apparition de symptômes de démence, compatible avec un rôle protecteur de ces cellules dans les tauopathies. Enfin, l’analyse post-mortem de cerveaux de patients atteints d’Alzheimer confirme la présence de Tau dans les tanycytes et révèle une altération marquée de leur structure : prolongements fragmentés et rupture de la communication LCS–sang. Cette dégradation semble spécifique à la maladie d’Alzheimer et n’est pas observée dans d’autres démences. Les auteurs en concluent que le dysfonctionnement des tanycytes pourrait favoriser l’accumulation de Tau et contribuer à la progression de la maladie, ouvrant la voie à de nouvelles pistes : préserver ou restaurer l’intégrité de ces cellules pourrait devenir une cible thérapeutique et, à terme, une stratégie de prévention.
SAUVE F et al., Tanycytic degeneration impairs tau clearance and contributes to Alzheimer’s disease pathology, Cell Press Blue, 2026; 1(1):100003
Vers un test du cancer du sein à domicile ?
Le cancer du sein, cancer le plus fréquemment diagnostiqué chez les femmes à l’échelle mondiale, reste une cause majeure de mortalité dans plus de 100 pays. Or, le diagnostic repose encore largement sur la mammographie, l’IRM et la biopsie, des examens qui peuvent être invasifs, coûteux ou difficiles d’accès selon les contextes, ce qui alimente l’intérêt pour des solutions de dépistage plus simples et non invasives.
Dans ce cadre, une équipe de l’université d’Aberystwyth (Pays de Galles, Royaume-Uni) développe un prototype de test urinaire à flux latéral, au format proche des tests de grossesse ou de dépistage de la Covid-19, destiné à être utilisé à domicile. Le dispositif vise à repérer dans l’urine des signatures biochimiques précoces liées au cancer du sein : l’approche s’appuie sur l’idée que certaines modifications métaboliques associées à la maladie produisent des composés excrétés et donc mesurables dans un échantillon facile à prélever.
Les chercheurs cherchent ainsi à transposer des résultats obtenus en laboratoire vers un outil « au chevet du patient » offrant une lecture simple, rapide et potentiellement abordable, avec l’objectif d’accélérer l’orientation diagnostique, de réduire le recours à des procédures invasives et, in fine, d’améliorer le pronostic grâce à une détection plus précoce.
Les travaux s’inscrivent dans un nouveau programme de recherche clinique de l’université combinant découverte de biomarqueurs et développement de prototypes, en collaboration avec des partenaires du NHS afin de passer plus vite de la preuve de concept à des usages pratiques. Le projet est soutenu par le programme SMART Award du gouvernement gallois et cofinancé par Dynamic Extractions Ltd, dont l’expertise en technologies de séparation complète les capacités analytiques et cliniques de l’équipe. Au-delà du cancer du sein, le même cadre de recherche translationnelle explore aussi des tests urinaires pour l’endométriose et le syndrome des ovaires polykystiques (SOPK), dans le but de réduire les retards de diagnostic en santé féminine.
Selon le professeur Luis Mur, les résultats mettent en évidence une signature biochimique détectable dès les stades très précoces, et la conversion en test à flux latéral pourrait aboutir à un outil accessible au plus grand nombre de femmes, tout en nécessitant les étapes habituelles de validation avant un déploiement en situation réelle.
AIMI-ZAINURIN NA et al., The Urinary Proteome Differs with the Presence and Type of Breast Cancer, Journal of Proteome Research, 2025; 24(12A):5932–5947, doi:10.1021/acs.jproteome.5c00229
MANIFESTATIONS
2026
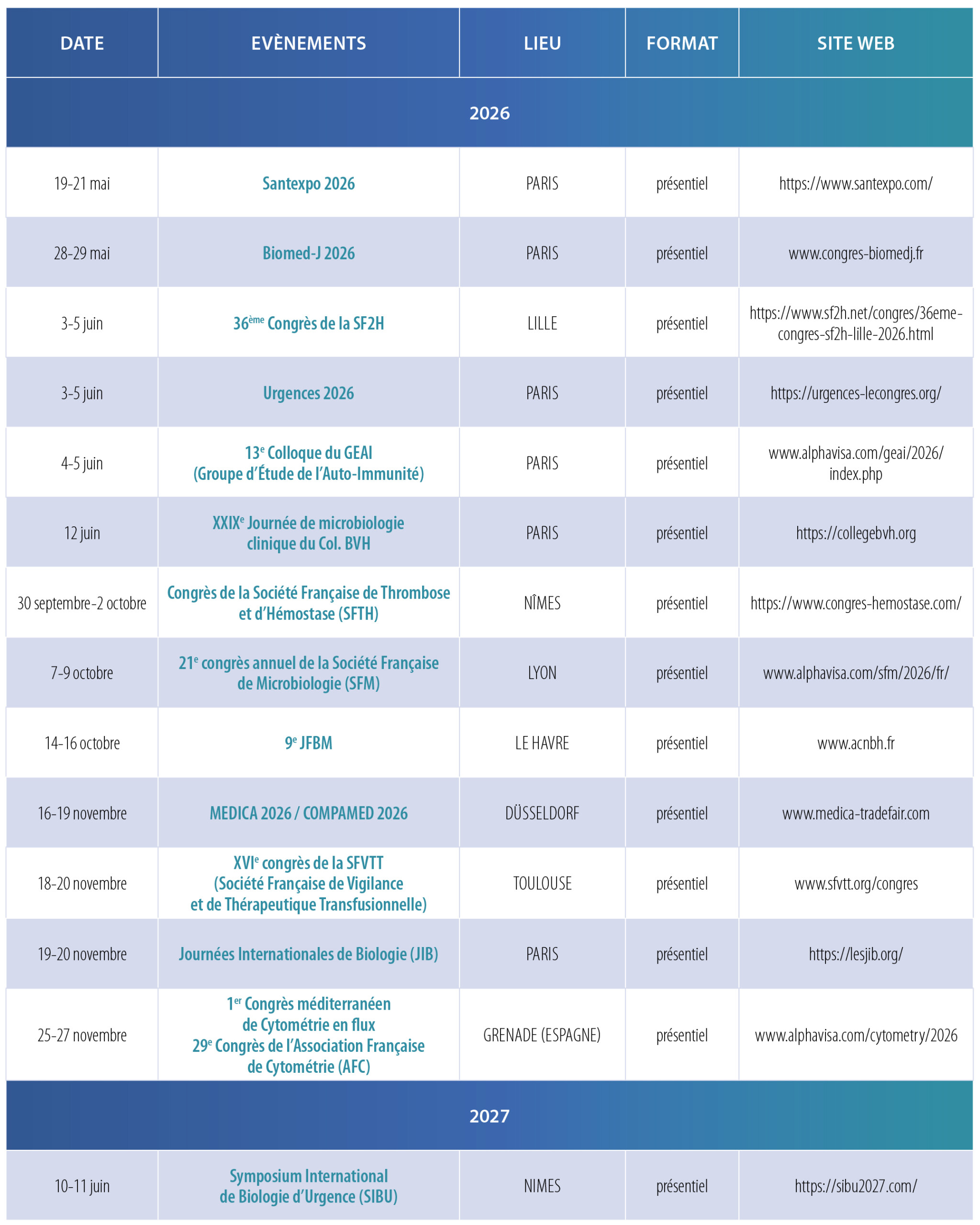
– 19-21 mai – Santexpo 2026 – PARIS – https://www.santexpo.com/
– 28-29 mai – Biomed-J 2026 – PARIS – www.congres-biomedj.fr
– 3-5 juin – 36ème Congrès de la SF2H – LILLE – https://www.sf2h.net/congres/36eme-congres-sf2h-lille-2026.html
– 3-5 juin – Urgences 2026 – PARIS – https://urgences-lecongres.org/
– 4-5 juin – 13e Colloque du GEAI (Groupe d’Étude de l’Auto-Immunité) – PARIS – www.alphavisa.com/geai/2026/index.php
– 12 juin – XXIXe Journée de microbiologie clinique du Col. BVH – PARIS – https://collegebvh.org
– 30 septembre-2 octobre – Congrès de la Société Française de Thrombose et d’Hémostase (SFTH) – NÎMES – https://www.congres-hemostase.com/
– 7-9 octobre – 21e congrès annuel de la Société Française de Microbiologie (SFM) – LYON – www.alphavisa.com/sfm/2026/fr/
– 14-16 octobre – 9e JFBM – LE HAVRE – www.acnbh.fr
– 16-19 novembre – MEDICA 2026 / COMPAMED 2026 – DÜSSELDORF – www.medica-tradefair.com
– 18-20 novembre – XVIe congrès de la SFVTT (Société Française de Vigilance et de Thérapeutique Transfusionnelle) – TOULOUSE – www.sfvtt.org/congres
– 19-20 novembre – Journées Internationales de Biologie (JIB) – PARIS – https://lesjib.org/
– 25-27 novembre – 1st Mediterranean Meeting on Flow Cytometry – GRENADE (ESPAGNE) – www.alphavisa.com/cytometry/2026
2027
– 10-11 juin – Symposium International de Biologie d’Urgence (SIBU) – NIMES – https://sibu2027.com/
Retrouvez dans Spectra Diagnostic N°44 :
BOURSE & BIOTECHS
XENON Pharmaceuticals, une valeur vivement recommandée par les analystes financiers
Erwan DURROUX, Yann DICKERSHEIT, Zoé REVERAND, Victor RAMARE, Arsia AMIR-ASLANI
BIOTECHNOLOGIES
Le Japon cherche à rattraper son retard dans le secteur des biotechnologies
Aurore WAFO, Andréa METRAUX, Ambre-Pacôme GAUTIER-AUDIGOU, Théo MAURIN, Arsia AMIR-ASLANI
MISE À JOUR DES CONNAISSANCES
Actualités sur les biomarqueurs de la maladie d’Alzheimer : vers une révolution diagnostique
Constance DELABY, Sylvain LEHMANN
CAS BIOCLINIQUES
Quiz
Benoit NESPOLA, Emeline VINATIER, Sophie DESPLAT-JEGO
CAS BIOCLINIQUES
Au-delà d’un résultat de laboratoire, une prestation de conseil biologique
Daniela LAKOMY
Newsletter Spectra Diagnostic N°43

IMMUNO-ANALYSE
Analyseur de chimiluminescence en auto-immunité et en allergie

Launch Diagnostics France SAS, distributeur indépendant de solutions de diagnostic médical, élargit son offre en annonçant la distribution en France de la gamme HOB BIOCLIA.
Développée par HOB Biotech, acteur reconnu en allergologie et en auto-immunité, la gamme Bioclia s’appuie sur une solide expertise industrielle et scientifique.
Au cœur de cette offre, le Bioclia 1900 est un analyseur de chimiluminescence entièrement automatisé, pensé pour répondre aux exigences actuelles des laboratoires en matière de rapidité, de performance et de gestion des flux.
Parmi ses caractéristiques clés, il délivre un premier résultat en 48 minutes, permettant une prise de décision rapide. Il repose sur une automatisation complète du processus analytique, associée à un chargement en continu des échantillons sans interruption des séries. Le système intègre également une gestion des échantillons STAT pour le traitement prioritaire des urgences, ainsi que des réactifs réfrigérés à bord, garantissant stabilité et continuité opérationnelle. Sa technologie de détection par chimiluminescence assure par ailleurs une haute sensibilité et une excellente spécificité analytique.
Le Bioclia 1900 propose un panel étendu de marqueurs couvrant notamment :
• Connectivites
• Vascularites
• Hépatite auto-immune
• Maladie cœliaque
• Diabète de type 1
• Dermatomyosite
• Syndrome des antiphospholipides
• Polyarthrite rhumatoïde
• Anémie pernicieuse
Cette large couverture pathologique permet d’accompagner les biologistes médicaux dans le diagnostic et le suivi des principales maladies auto-immunes, tout en optimisant les flux analytiques au sein du laboratoire. Elle offre également l’opportunité de consolider l’activité d’auto-immunité sur un système unique, avec un impact positif sur l’organisation et la
rationalisation des équipements.
Grâce à cette nouvelle distribution, Launch Diagnostics France SAS renforce son engagement à fournir des solutions technologiques innovantes, robustes et adaptées aux besoins du marché français. L’intégration de cet automate à son portefeuille s’inscrit dans une volonté d’accompagner les laboratoires dans l’optimisation de leurs performances analytiques et organisationnelles, au service d’une meilleure prise en charge des patients.
Launch Diagnostics France SAS présentera le Bioclia 1900 lors du prochain congrès du GEAI, les 4 et 5 juin 2026, et sera présent avec HOB au 15e Congrès international d’auto-immunité, qui se tiendra à Prague en mai prochain. Ces rendez-vous seront l’occasion d’échanger avec les professionnels du secteur et de présenter les performances du système.
INFORMATIQUE DE LABORATOIRE
Génération automatique de comptes-rendus vulgarisés
Dedalus, acteur européen majeur des logiciels pour les établissements de santé et les laboratoires de biologie médicale et d’anatomopathologie, annonce un partenariat stratégique avec Vulgaroo, startup française spécialisée dans la vulgarisation des documents médicaux pour les patients.
Dedalus a présenté la version 5.5 de son InVitro Patient Portal, dans laquelle la solution « Vulgaroo by Dedalus » est désormais intégrée et proposée comme fonctionnalité innovante activable sur demande des laboratoires.
La société Vulgaroo s’est donné comme mission de rendre les données de santé, par nature complexes, compréhensibles pour les patients. Pour accomplir cette mission, elle croise IA génératives, données de santé labellisées, expertise médicale et voix des patients.
Concrètement, elle a développé une plateforme web et des APIs capables de générer automatiquement des “Mémos Patients” à partir de comptes-rendus médicaux. Les mémos doivent fournir des informations claires, pédagogiques et compréhensibles, et sont accessibles directement sur le portail patient Dedalus.
En intégrant cette solution à son InVitro Patient Portal, l’éditeur poursuit son ambition de couvrir l’ensemble de la chaîne de la biologie, du préanalytique au postanalytique, tout en renforçant la dimension servicielle de son offre digitale. Ces mémos constituent également un levier d’adoption des outils numériques déjà proposés via le portail (prise de rendez-vous en ligne, paiement du reste à charge, consultation sécurisée des résultats, etc.).
Frédéric Poirier, Directeur de la Business Unit Diagnostic In Vitro chez Dedalus France : « En l’intégrant à notre InVitro Patient Portal, nous permettons à nos clients de déployer facilement ce Mémo Patient auprès de leur patientèle. Généré automatiquement dans la continuité du compte rendu médical et accessible directement dans l’espace résultats, il crée de la valeur pour le patient tout en renforçant l’adoption des outils numériques du laboratoire. »
L’accord permet à Vulgaroo de proposer sa solution auprès de plus de 4 000 laboratoires en France.
Le recours massif des patients aux sources d’information numériques (ChatGPT et autres LLM, réseaux sociaux, forums santé etc.) présente un risque en termes de fuite des données et de désinformation médicale – l’information restant souvent trop complexe et non vérifiée. Dans ce contexte, Vulgaroo veut se différencier avec une solution française souveraine, validée par des professionnels de santé et des patients, et conforme aux réglementations en matière de santé et de cybersécurité (RGPD, IA Act, HDS).
INFORMATIQUE DE LABORATOIRE
16 nouvelles analyses pour le système expert d’aide à la validation biologique
Le pôle biologique de la société Valab, en collaboration avec des laboratoires de biologie médicale français et suisses, ont modélisé 16 nouvelles analyses réparties en cinq spécialités (oligo-éléments, biochimie, gaz du sang, biologie moléculaire et biomarqueurs). Une évolution qui reflète l’engagement de la société à proposer de nouvelles analyses pour augmenter les performances et l’expertise de leur logiciel Valab®. Les nouvelles analyses modélisées, ajoutées au catalogue, sont les suivantes :
– Oligo-éléments (nouvelle spécialité)
• Le cuivre sanguin et urinaire, le zinc, le sélénium et le manganèse : Oligo-éléments essentiels pour le bon fonctionnement du métabolisme.
• Céruléoplasmine : protéine plasmatique assurant le transport du cuivre dans le sang.
– Biomarqueurs (spécialité Biochimie)
• CTX et Ostéocalcine : marqueurs osseux utilisés notamment dans le cadre de l’ostéoporose.
• Protéine S100B : biomarqueur de lésion cérébrale utilisé dans les laboratoires hospitaliers afin d’éviter des scanners cérébraux non nécessaires lors de traumatismes crâniens.
• Calprotectine : biomarqueur pour détecter et suivre l’inflammation intestinale des maladies inflammatoires chroniques de l’intestin (MICI) et éviter dans certains cas des coloscopies. Cette analyse est désormais remboursée par la sécurité sociale sur prescription médicale.
• Cystatine C : biomarqueur de la fonction rénale indépendant de la masse musculaire du patient.
– Bactériologie
• PCR de Chlamydia et Gonorrhée : analyses utilisées dans le dépistage des infections sexuellement transmissibles (IST), remboursées sur prescription médicale.
– Gaz du sang
• FiO₂, ratio PO₂/FiO₂ et température corporelle : analyses utilisées lors de l’exploration de l’insuffisance respiratoire.
Par ces enrichissements, la société souhaite permettre aux utilisateurs de suivre les tendances de la biologie médicale. Le catalogue comprend aujourd’hui plus de 350 analyses clé en main, il est consultable et téléchargeable directement sur le site web, ou disponible sur simple demande auprès de la société. De nouvelles analyses sont déjà en cours de préparation et viendront compléter prochainement le panel.
MATERIEL DE LABORATOIRE
Connectivité Wi-Fi sécurisée conçue pour la surveillance

Dickson a conçu le nouveau Cobalt XS Wi-Fi pour simplifier la surveillance environnementale dans les environnements critiques. Compact et intuitif, ce nouveau produit vient compléter la gamme Cobalt X/XS, leader sur le marché, et offre la puissance du Wi-Fi dans un format facile à utiliser avec une connectivité universelle.
Avec ce nouveau dispositif, la surveillance avancée de la température, de l’humidité et d’autres paramètres physiques est facile à déployer dans toutes les installations : il suffit d’une connexion Wi-Fi. L’appareil est entièrement conforme aux normes GxP et offre un accès complet à tous les avantages de la plateforme logicielle OCEAView.
Il prend en charge la technologie Smart Sensor de Dickson, qui facilite les opérations d’étalonnage en stockant toutes les informations directement dans le capteur. Cela permet à la fois une précision constante et un remplacement rapide des capteurs sans interruption de la surveillance. Grâce à cette nouvelle architecture, il garantit la précision, la traçabilité et la sécurité des données.
Rick Weiler, PDG de Dickson : « Les clients peuvent désormais ajouter des enregistreurs de données là où le Wi-Fi est déjà disponible afin de compléter nos applications d’enregistreurs de données LoRa. »
Connectivité Wi-Fi sans effort
• Taille compacte : 69 x 107 x 31 mm, pour un poids de 130 g
• Jusqu’à 32 000 mesures par capteur stockées localement
• Alertes instantanées et visualisation en temps réel via les plateformes Dickson Cloud
• Alimentation par batterie, éliminant le besoin d’une passerelle ou d’une configuration réseau
• Écran LCD haute visibilité pour une lecture immédiate des données
• Connexion Wi-Fi 2,4 GHz compatible avec les dernières normes (Wi-Fi 5 et Wi-Fi 6).
Conçu pour les applications critiques
Que ce soit pour les réfrigérateurs, les congélateurs, les salles blanches, les laboratoires, les entrepôts ou les équipements industriels, Cobalt XS Wi-Fi offre une grande flexibilité dans le déploiement et la mise à l’échelle de la surveillance de la température.
• Polyvalence et adaptabilité : convient à de multiples environnements, installations et capteurs, avec des rapports fiables et précis
• Facilité d’installation : mise en service immédiate grâce à une connexion Wi-Fi standard
• Interface intuitive : assure une surveillance continue et ininterrompue des produits critiques sensibles à la température.

25 acteurs d’excellence unissent leurs forces dans l’Appel de Paris Saclay pour une Europe souveraine par la science

Lancé le jeudi 19 février 2026, en clôture du 3e Paris-Saclay Summit, l’Appel de Paris-Saclay rassemble un consortium inédit d’universités et alliances – France Universités, Institut Polytechnique de Paris, Université Paris-Saclay – d’instituts de recherche – CEA, CNRS, INRAE, INRIA, INSERM, Institut Curie, Institut Imagine, Institut Pasteur – et d’entreprises telles que Danone, EDF, Equans, Sanofi.
Depuis, en une semaine, les soutiens se sont multipliés de manière spectaculaire : l’Onera, les entreprises Exotrail, Kimialys, Quandela, STMicroelectronics ; à l’international, Aarhus University (Danemark), EIFER – European Institute for Energy Research (Allemagne), Wageningen University & Research (Pays-Bas), les élus de premier plan de l’Île-de-France, Valérie Pécresse, Présidente de la Région, François Durovray, Président du Département de l’Essonne et Grégoire de Lasteyrie, Président de l’agglomération Paris-Saclay.
L’Appel de Paris-Saclay constitue un signal stratégique à la veille des négociations décisives sur FP10, le futur programme-cadre européen doté de 175 milliards d’euros (2028-2034).
Le consortium influencera les négociations FP10 (mars-mai 2026), l’évaluation Horizon Europe (septembre 2026) et le budget UE 2028-2034, avec un premier bilan lors de la prochaine édition du Paris-Saclay Summit, début 2027.
L’Appel de Paris-Saclay commence ainsi :
« Nous, acteurs académiques, organismes de recherche, universités, centres technologiques et entreprises privées engagées en R&D, souhaitons adresser un appel solennel aux décideurs des États membres et aux institutions de l’Union européenne. Les décisions qui seront prises dans les prochains mois concernant le financement, l’architecture et la mise en œuvre du futur programme-cadre européen FP10 structureront durablement la capacité de l’Europe à produire des connaissances, transformer l’excellence scientifique en innovations, et affirmer sa souveraineté stratégique. »
Pour Grégoire de Lasteyrie, Président de l’agglomération Paris-Saclay, « L’Appel de Paris-Saclay est un acte fort et collectif ! Un engagement total pour la science et pour une Europe plus forte. Nous devons enrayer le décrochage technologique qui menace notre continent mais aussi faire face aux dynamiques impérialistes qui déstabilisent l’ordre mondial.
À Paris-Saclay, nous faisons un choix clair, celui de transformer ces crises en opportunités historiques. La science doit être le moteur de la stratégie de renforcement de la souveraineté européenne, pour les prochaines décennies. »
Un agenda en cinq priorités stratégiques
Cet appel solennel cible les faiblesses d’Horizon Europe (valorisation timide, déséquilibres nationaux) et prolonge les rapports Draghi (R&D-industrie), Letta (cinquième liberté des savoirs) et Heitor (Choose Europe). Ses axes :
1. Atteindre l’échelle européenne pour des projets massifs (ex. : réseaux d’essais cliniques).
2. Préserver la liberté académique, identité attractive de l’Europe.
3. Renforcer le continuum recherche-industrie (24 des 28 médicaments majeurs issus de fonds publics).
4. Maîtriser les technologies critiques : IA, quantique, santé, énergie, spatial, défense.
5. Coordonner les stratégies nationales et européennes (90 % des fonds publics décidés localement).
« La science abolit les frontières par essence. L’Europe est l’arène impérative pour partager risques, expertises et outils, érigeant une Union techniquement indépendante », renchérit Sylvie Retailleau, Présidente d’Universcience et ancienne ministre de l’Enseignement Supérieur et de la Recherche.
Paris-Saclay, berceau naturel de l’Appel
Paris-Saclay, territoire unique, concentre 20 % de la recherche publique et privée française et conjugue excellence académique, puissance industrielle et infrastructures d’avant-garde.
L’Université Paris-Saclay et l’Institut Polytechnique de Paris, deux pôles de rang mondial, animent son cœur scientifique.
Plus de 300 laboratoires d’envergure internationale y produisent des savoirs critiques.
Parmi ses atouts majeurs : l’IRM 11,7 Tesla de NeuroSpin (n°1 mondial en neurosciences), le synchrotron SOLEIL (analyse de matériaux, unique en Europe), le supercalculateur Jean-Zay (n°1 continental), les calculateurs quantiques de Quandela (pionniers européens).
Avec plus de 600 startups deeptech, Paris-Saclay transforme la science en succès économiques et industriels au service de la souveraineté européenne.
Paris-Saclay Summit : un succès sans précédent
À l’initiative de l’agglomération Paris-Saclay, co-organisé avec Le Point, la Région Île-de-France et le Département de l’Essonne, le Paris-Saclay Summit fait depuis trois ans de Paris-Saclay la capitale européenne de la science pendant deux jours intenses.
Les 18 et 19 février 2026 ont marqué une édition record : 5 000 participants, 25 000 réservations de conférences (moyenne de 5 par personne), en hausse de 45 % versus 2025.
130 scientifiques de 20 nationalités ont animé 80 sessions, avec des intervenants d’exception : le Prix Nobel Didier Queloz (exoplanètes), Valérie Masson-Delmotte et Jean Jouzel (climat), Eugenia Cheng et Stéphane Mallat (mathématiques), Michael E. Mann (paléoclimat), sans oublier le Palmarès des 100 Inventeurs du Point.
Ce furent également des engagements emblématiques : auprès des jeunes avec « La Recherche en Baskets » et les nombreux échanges entre intervenants et étudiants ; auprès des femmes avec une parité absolue dans les prises de parole et l’inauguration de l’observatoire territorial des inégalités liées au genre dans l’orientation des lycéens et lycéennes (Fondation Université Paris-Saclay) ; auprès de la recherche et de l’Europe avec l’Appel de Paris-Saclay.
La division Biosciences et Diagnostic de BD passe chez Waters
Waters Corporation a finalisé la fusion avec les activités Biosciences et Solutions de diagnostic de Becton, Dickinson and Company (BD), créant ainsi un leader mondial dans les sciences de la vie et le diagnostic. Ce rapprochement stratégique vise à renforcer la position de Waters sur le marché en réunissant des technologies de pointe et une expertise scientifique reconnue dans les domaines de la chimie, de la biologie et de la physique. La transaction s’accompagne également de la nomination du Dr Claire M. Fraser, Ph.D., scientifique éminente spécialisée dans le génome, au conseil d’administration, qui compte désormais 11 membres.
Claire M. Fraser apporte trois décennies d’expérience dans la gestion d’instituts de recherche, notamment en tant que fondatrice et directrice de l’Institut des sciences du génome à l’Université du Maryland, où elle a également été professeure de médecine, de microbiologie et d’immunologie. Son expertise en génomique, maladies infectieuses et diagnostic moléculaire est saluée comme un atout majeur pour l’orientation stratégique de Waters.
Le président-directeur général, Udit Batra, souligne que l’association avec BD marque un tournant pour répondre aux besoins non satisfaits des clients, créer de la valeur à long terme pour les actionnaires et apporter des solutions innovantes pour la santé mondiale.
Suite à la clôture de la transaction, Waters a réorganisé ses activités en quatre divisions distinctes :
• Waters Analytical Sciences : spécialisée dans la science de la séparation et la caractérisation moléculaire, incluant chromatographie liquide, spectrométrie de masse, analyse des particules et technologies associées.
• Waters Biosciences : centrée sur la biologie, le tri et l’analyse cellulaires, notamment la cytométrie de flux et les solutions multiomiques à cellule unique.
• Waters Advanced Diagnostics : dédiée aux diagnostics à haute valeur ajoutée dans les environnements cliniques, couvrant microbiologie, tests moléculaires, multiplex LC-MS, automatisation et tests sur le lieu de soins.
• Waters Materials Sciences : couvrant l’analyse thermique, la rhéologie et la microcalorimétrie pour des secteurs comme les batteries, l’électronique et la pharmacie.
Cette nouvelle organisation vise à favoriser l’innovation, soutenir le développement de produits thérapeutiques, et accélérer la croissance sur des marchés adjacents à forte expansion. Waters s’appuie sur des équipes scientifiques de haut niveau pour répondre à des besoins variés, des tests alimentaires et environnementaux aux diagnostics spécialisés.
En résumé, la fusion entre Waters et BD marque une étape majeure pour l’entreprise, qui mise sur l’excellence scientifique, la diversité de ses divisions et l’innovation pour renforcer sa position internationale.
PROFESSION
Maladies cardiométaboliques : 3e campagne de sensibilisation de l’IHU ICAN
Le concept de maladies cardiométaboliques met en lumière une réalité encore trop peu connue dans la population : la majorité des maladies cardiovasculaires trouvent leur origine dans des troubles métaboliques. Diabète, obésité, stéatose hépatique métabolique (MASH), dyslipidémies ou hypertension constituent un ensemble de pathologies étroitement liées qui favorisent la survenue d’événements cardiovasculaires. En France, les maladies cardiovasculaires sont la deuxième cause de mortalité, avec près de 140 000 décès chaque année. Plus de 73 % de cette mortalité est associée à une cause métabolique.
« Nous ne pouvons plus accepter que le lien entre ces maladies reste sous les radars. Les maladies cardiométaboliques sont une cause majeure de mortalité alors qu’elles sont en grande partie évitables. Pourtant, elles ne bénéficient pas d’autant de visibilité que d’autres maladies comme les cancers par exemple. 70 % des Français n’ont jamais entendu parler des maladies cardiométaboliques selon le baromètre 2025 IFOP/IHU ICAN. Il est urgent de changer d’échelle dans la prévention. Les maladies cardiométaboliques ne sont pas une fatalité biologique. Elles sont le reflet de nos modes de vie, de nos environnements et de nos choix collectifs » explique le Pr Stéphane Hatem, Directeur général de l’IHU ICAN.
C’est pourquoi l’IHU ICAN se mobilise, du 30 mars au 19 avril 2026, en déployant la 3e édition de sa campagne de sensibilisation qui a pour objectif principal d’apporter une information claire sur les maladies cardiométaboliques au grand public grâce à des actions concrètes et accessibles comme des webinaires, une journée de prévention cardiométabolique ouverte à tous à la Pitié-Salpêtrière le 13/04 de 10h à 16h, un challenge connecté ICAN GO pour promouvoir l’activité physique du 30/03 au 19/04 et des «Fresques de l’obésité» pour mieux connaitre cette maladie, les 7/04, 16/04 et 17/04.
De nombreuses associations de patients et partenaires institutionnels se sont engagés pour relayer cette campagne : l’AP-HP, la CNAM, Santé publique France, Sorbonne Université, l’Inserm, l’association Poids Plumes France, SOS hépatites et Maladies du foie, l’Amicale des transplantés de la Pitié-Salpêtrière, Anhet, la Fédération Française des Diabétiques.
Situé au cœur de l’hôpital de la Pitié-Salpêtrière à Paris, l’IHU ICAN est un pôle d’excellence dans le domaine des maladies cardiométaboliques (diabète, obésité, dyslipidémies, MASH, maladies cardiovasculaires). Porté par l’AP-HP, l’Inserm et Sorbonne Université, il rassemble des experts de renommée internationale et des technologies de pointe : 168 médecins, 221 chercheurs, 75 études cliniques en cours, 6 centres de
référence maladies rares, 4 parcours de soin innovants, plus de 7000 publications scientifiques et plus de 42 000 patients inclus dans des cohortes, registres et essais cliniques.
Programme et modalités
Institut de Cardiométabolisme et Nutrition, IHU ICAN
Expérimentation du remboursement des analyses de soumission chimique
Depuis le 1er janvier 2026, une expérimentation majeure est lancée dans trois régions françaises (Hauts-de-France, Île-de-France, Pays de la Loire), visant le remboursement des examens de biologie médicale pour détecter une soumission chimique, même sans dépôt de plainte préalable. Cette initiative, revendiquée par la députée Sandrine Josso et la sénatrice Véronique Guillotin dans leur rapport de mai 2025, répond à un besoin crucial d’améliorer l’accès aux analyses et de lutter contre l’errance diagnostique pour les victimes potentielles.
Suite à l’amendement déposé dans le PLFSS 2024, la mesure est adoptée via l’article 68 de la LFSS 2025 pour une durée de trois ans, avec une extension prévue en Guadeloupe. Dans chaque région concernée, un laboratoire spécialisé (CHI de Lille, hôpital Raymond-Poincaré de l’AP-HP, CHU de Nantes) est chargé d’analyser les échantillons prélevés et de conserver les échantillons non utilisés pendant trois ans, permettant ainsi d’éventuelles contre-expertises judiciaires.
Hors expérimentation, les examens ne sont pas remboursés par l’Assurance maladie, sauf dans le cadre d’une plainte où ils sont pris en charge au titre des frais de justice. Le coût élevé de ces analyses (jusqu’à 1 200 euros) constituait jusqu’ici un obstacle majeur à la prise en charge des victimes.
La ministre de la Santé, Stéphanie Rist, a salué ce dispositif qui, selon elle, marque « une nouvelle étape déterminante de la politique gouvernementale de lutte contre toutes les formes de violences faites aux femmes » et garantit un accès simplifié et inconditionnel aux analyses médicales pour les victimes potentielles.
Pour bénéficier de l’expérimentation, il suffit de présenter une ordonnance d’un médecin de l’une des trois régions pilotes, précisant l’expérimentation. Après entretien clinique, le médecin prescrit les examens (sang, urines, cheveux) s’il les juge justifiés. Le patient reçoit alors une note d’information, une fiche de liaison, un formulaire de consentement à la transmission des résultats et à la conservation des échantillons. Les résultats sont adressés au médecin prescripteur, qui les explique au patient lors d’une consultation dédiée.
Le décret prévoit également la possibilité de protocoles locaux permettant aux infirmiers de prescrire et réaliser les prélèvements. Enfin, un rapport d’évaluation sera transmis au Parlement six mois avant la fin de l’expérimentation, afin de décider d’une éventuelle généralisation du dispositif à toute la France.
Alzheimer : l’implication majeure des tanycytes révélée

Les tanycytes (en blanc) capturent la protéine Tau (rouge) circulant dans le LCS pour la transporter le long de leurs prolongements/bras qui traversent le tissu cérébral et entrent en contact avec les vaisseaux sanguins (en vert) dans lesquels ils déversent cette protéine impliquée dans la pathologie d’Alzheimer lorsqu’elle s’accumule dans le cerveau. © Vincent Prévot/Inserm
Des chercheurs de l’Inserm, de l’Université de Lille et du CHU de Lille ont mis en lumière le rôle des tanycytes dans la maladie d’Alzheimer. Cette pathologie s’accompagne d’une accumulation anormale de la protéine Tau dans le cerveau. Normalement, Tau est sécrétée par les neurones et éliminée dans le sang via le liquide cérébrospinal (LCS). Mais chez les patients malades, Tau s’accumule sous une forme pathologique, entraînant la dégénérescence neuronale et le déclin cognitif.
Les mécanismes expliquant cette accumulation restaient obscurs. Les tanycytes, cellules facilitant les échanges entre le sang et le LCS, étaient jusqu’ici surtout connues pour leur rôle dans le transport d’hormones comme la leptine. Grâce à une approche expérimentale innovante, les chercheurs ont démontré que les tanycytes capturent la protéine Tau dans le LCS et l’acheminent vers les capillaires sanguins. En bloquant le fonctionnement des tanycytes chez l’animal, ils ont observé une forte diminution de l’évacuation de Tau vers le sang, confirmant leur rôle central dans ce processus.
De plus, chez des souris présentant une accumulation de Tau, l’inhibition des tanycytes a accéléré l’apparition de symptômes de démence. L’étude de cerveaux humains post-mortem a révélé que les tanycytes étaient altérées chez les patients Alzheimer, avec des prolongements fragmentés. Ce phénomène n’est pas observé dans d’autres types de démence. Ces observations suggèrent que la dégradation des tanycytes contribue à l’accumulation pathologique de Tau et donc à la progression de la maladie.
Pour la première fois, ces résultats pointent les tanycytes comme une cible thérapeutique potentielle. Préserver leur intégrité pourrait, à terme, permettre de freiner ou de prévenir le développement d’Alzheimer, ouvrant ainsi de nouvelles pistes de recherche et d’intervention contre cette maladie.
SAUVE F et al., Tanycytic degeneration impairs tau clearance and contributes to Alzheimer’s disease pathology, Cell Press Blue, 2026; Online, doi:10.1016/j.cpblue.2026.100003
Maladies cardiovasculaires : deux examens plus précis pour l’athérosclérose
Une étude a démontré que la réalisation de deux examens spécifiques pour dépister l’athérosclérose permet de mieux évaluer le risque de maladies cardiovasculaires, même chez les personnes sans symptômes et considérées à faible ou moyen risque.
Créé en 1995, le Centre de Dépistage et de Prévention de l’Athérosclérose (CDPA) du CHU de Toulouse propose aujourd’hui deux examens pour évaluer la présence de dépôts dans les artères, signes d’athérosclérose et de lésions cardiovasculaires : (i) depuis 1995, une prise de sang pour mesurer la lipoprotéine (a), (ii) et, depuis 2015, le scanner cardiaque sans injection pour mesurer le calcium des artères coronaires (score calcique ou score d’Agatston).
Afin d’accompagner les médecins dans une démarche d’évaluation du risque cardiovasculaire en prévention primaire, des scores de risque cardiovasculaire ont été développés : ces outils combinent plusieurs facteurs de risque reconnus afin d’estimer le risque à 10 ans.
Parmi eux, le Score2, recommandé par la Société Européenne de Cardiologie, prend en compte l’âge, le sexe, le tabagisme, la tension artérielle et le taux de cholestérol. Il permet de classer le risque cardiovasculaire en quatre niveaux — faible, modéré, élevé ou très élevé — et d’orienter ainsi sur les mesures de prévention nécessaires (conseils d’hygiène de vie ou traitement).
L’étude a analysé les données de 3 442 patients suivis au CDPA, à l’aide des deux examens. Les résultats montrent que :
• de nombreux patients présentent déjà des dépôts dans leurs artères, révélés par un score calcique élevé, même parmi ceux initialement classés à faible ou moyen risque.
• un taux élevé de la lipoprotéine (a) est fréquemment observé chez ces patients, ce qui permet de mieux stratifier le risque et d’identifier les patients qui bénéficieront d’un traitement préventif, notamment par statines pour réduire le cholestérol.
Selon les recommandations basées sur le Score2, la prescription de statines est recommandée chez 21,6 % des patients à risque bas ou intermédiaire, 83,5 % des patients à risque élevé, 93,2 % des patients à très haut risque. Grâce à l’analyse de leur score coronaire calcique et de leur taux de lipoprotéine (a), ces pourcentages passent respectivement à 15,5 %, 35,3 %, et 35,8 %.
Selon le Pr Jean Ferrières, cardiologue (CHU de Toulouse) et le Dr Anthony Matta, cardiologue (CH intercommunal des vallées de l’Ariège) le Score2 doit rester le test de premier intention : gratuit et rapide, il favorise une prise en charge spécialisée précoce et adaptée. Néanmoins, en cas de doute sur la nécessité d’un traitement préventif à long terme, le calcul du score coronaire calcique d’Agatston et le dosage de la lipoprotéine (a) apportent une réelle valeur ajoutée.
MATTA A et al., Comparison of primary prevention strategy guided by SCORE2 versus coronary artery calcium scoring in a non-diabetic population, Eur J Intern Med, 2026, Online, doi:10.1016/j.ejim.2026.106700
MANIFESTATIONS
2026
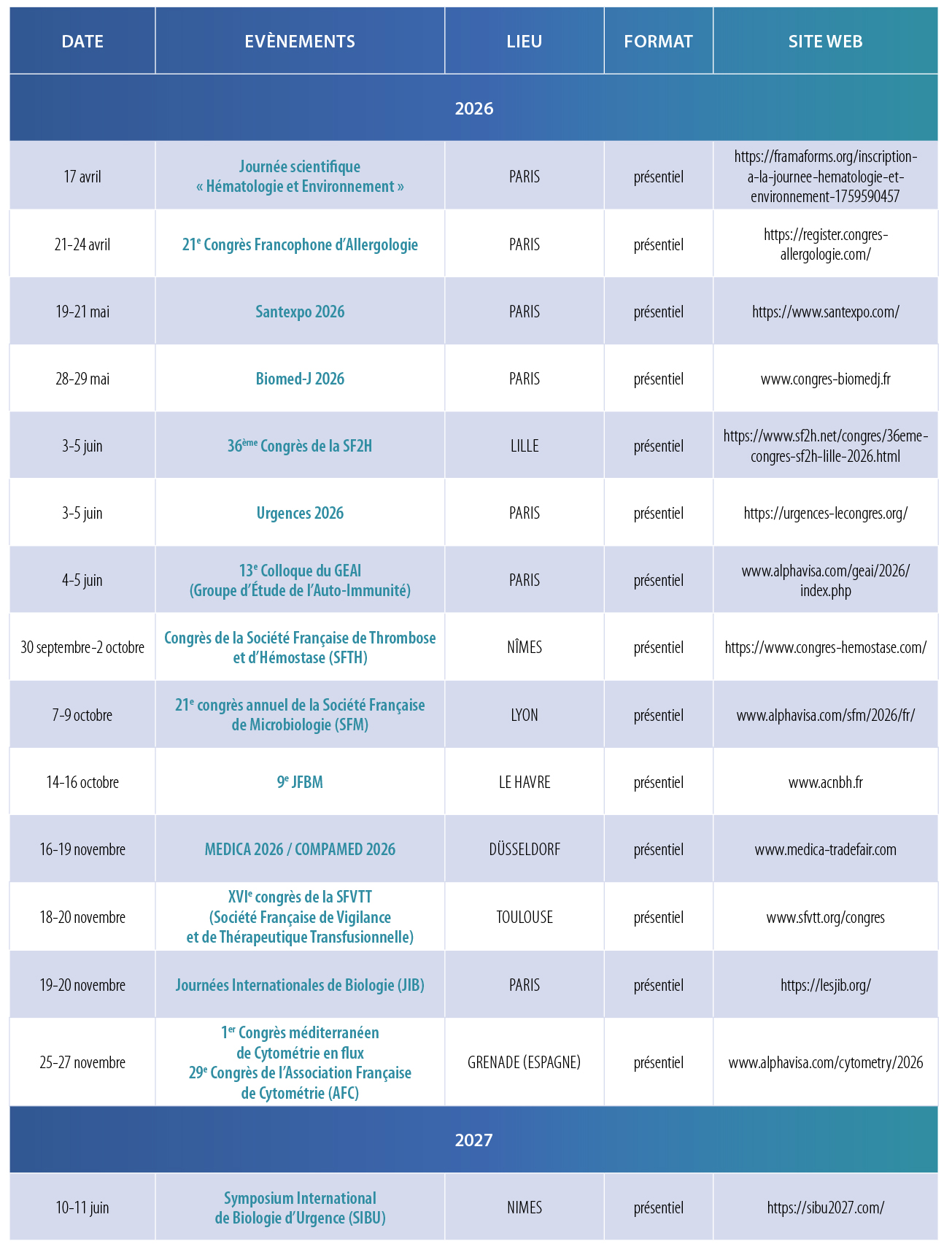
– 17 avril – Journée scientifique « Hématologie et Environnement » – PARIS – https://framaforms.org/inscription-a-la-journee-hematologie-et-environnement-1759590457
– 21-24 avril – 21e Congrès Francophone d’Allergologie – PARIS – https://register.congres-allergologie.com/
– 19-21 mai – Santexpo 2026 – PARIS – https://www.santexpo.com/
– 28-29 mai – Biomed-J 2026 – PARIS – www.congres-biomedj.fr
– 3-5 juin – 36ème Congrès de la SF2H – LILLE – https://www.sf2h.net/congres/36eme-congres-sf2h-lille-2026.html
– 3-5 juin – Urgences 2026 – PARIS – https://urgences-lecongres.org/
– 4-5 juin – 13e Colloque du GEAI (Groupe d’Étude de l’Auto-Immunité) – PARIS – www.alphavisa.com/geai/2026/index.php
– 30 septembre-2 octobre – Congrès de la Société Française de Thrombose et d’Hémostase (SFTH) – NÎMES – https://www.congres-hemostase.com/
– 7-9 octobre – 21e congrès annuel de la Société Française de Microbiologie (SFM) – LYON – www.alphavisa.com/sfm/2026/fr/
– 14-16 octobre – 9e JFBM – LE HAVRE – www.acnbh.fr
– 16-19 novembre – MEDICA 2026 / COMPAMED 2026 – DÜSSELDORF – www.medica-tradefair.com
– 18-20 novembre – XVIe congrès de la SFVTT (Société Française de Vigilance et de Thérapeutique Transfusionnelle) – TOULOUSE – www.sfvtt.org/congres
– 19-20 novembre – Journées Internationales de Biologie (JIB) – PARIS – https://lesjib.org/
– 25-27 novembre – 1st Mediterranean Meeting on Flow Cytometry – GRENADE (ESPAGNE) – www.alphavisa.com/cytometry/2026
2027
– 10-11 juin – Symposium International de Biologie d’Urgence (SIBU) – NIMES – https://sibu2027.com/
Retrouvez dans Spectra Diagnostic N°43 :
BOURSE & BIOTECHS
La performance boursière de Genfit : Against All Odds (Contre Toute Attente)
Helena SWINNEN, Emma MARONGIU, Thirathada CHINCHAPO, Serena ISAAC, Arsia AMIR-ASLANI
BIOTECHNOLOGIES
La Chine : l’émergence d’un nouveau géant dans le secteur des biotechnologies
Arthur BASMANDJIAN, Abigail DE MIRAS, Robin FOURMANOIR, Thibault VANOOST, Clémence THOREL, Arsia AMIR-ASLANI
BIOTECHNOLOGIES
Abivax, la pépite française suscite beaucoup de convoitise de la part des géants pharmaceutiques
Noah BUI, Gizem YILDIRIM, Arsia AMIR-ASLANI
CAS BIOCLINIQUES
Place des tests dans le dépistage de l’infection au VIH : à propos d’un cas
Ylhame Kahina SOUAMI
CONSEILS
Prenez le contrôle de vos finances et de votre patrimoine avant que les choix ne se fassent sans vous
Bruno SAVIANA
Newsletter Spectra Diagnostic N°42

ALLERGIES
Neuf nouveaux allergènes disponibles, dont six ciblant les arachides

Siemens Healthineers a élargi son menu de tests 3gAllergy avec neuf nouveaux allergènes, dont six ciblant les arachides, principale cause d’anaphylaxie mortelle liée à l’alimentation. Des composants dérivés des acariens et du blé sont également désormais disponibles. Les informations délivrées permettent aux cliniciens de mieux distinguer les sensibilisations à haut risque des expositions plus bénignes, contribuant ainsi à orienter les soins prodigués aux patients de manière plus personnalisée et mieux informée. Ces ajouts portent à plus de 500 le nombre total d’allergènes disponibles sur le système IMMULITE 2000 XPi.
Le test 3gAllergy de Siemens Healthineers est un test IgE spécifique aux allergènes qui aide les médecins à identifier, surveiller et prendre en charge les patients atteints de maladies allergiques. Les neuf nouveaux allergènes ajoutés au menu 3gAllergy sont marqués CE et sont désormais largement disponibles.
Les tests de composants allergènes spécifiques fournissent des informations précieuses aux cliniciens et aux personnes souffrant d’allergies. On estime que 30 à 40 % de la population mondiale souffre d’une ou plusieurs allergies. Si les tests d’allergie standard confirment la présence d’une allergie, les informations au niveau des composants aident les médecins à élaborer des stratégies de gestion des allergies plus personnalisées. Cette approche contribue à améliorer la qualité de vie en minimisant les restrictions potentiellement inutiles. Par exemple, au lieu d’éviter complètement les arachides, les personnes allergiques peuvent faire des choix plus précis en fonction de leurs risques spécifiques de réaction indésirable.
INFORMATIQUE DE LABORATOIRE
Assurer la continuité du diagnostic en laboratoire
Dans un laboratoire, la moindre interruption du Système d’Information de Laboratoire (SIL) peut entraîner des retards de production, perturber les équipes techniques et, surtout, impacter la qualité du service rendu aux patients. C’est pourquoi Data Innovations a développé Backup SIL, un module conçu pour garantir la continuité des activités diagnostiques, même en cas de défaillance du système principal.
Ce module s’intègre directement au serveur Instrument Manager (IM), avec lequel il partage la même base de données. Cette architecture permet ainsi un accès immédiat aux données essentielles (patients, prescripteurs et analyses), une mise à jour continue, pour une synchronisation parfaite et un déploiement rapide, ne nécessitant aucune infrastructure supplémentaire. Grâce à cette intégration native, le système demeure opérationnel à tout moment, même dans les situations critiques.
Lorsque le SIL principal tombe en panne, Backup SIL prend instantanément le relais. Après la saisie des demandes, celles-ci sont automatiquement transmises à Instrument Manager, qui assure l’envoi des analyses vers les automates, la production et la gestion des résultats, puis la remontée des données dans Backup SIL après validation technique.
Cette chaîne de traitement continue garantit une production sans interruption. Conçu pour l’efficacité en situation d’urgence, ce module propose une interface intuitive pensée pour une saisie rapide : identification sécurisée des patients via l’IPP, panels d’analyses préconfigurés, traçabilité complète (médecins, services, heure de prélèvement), impression instantanée des étiquettes de tubes.
Ces fonctionnalités permettent aux techniciens de maintenir leur niveau de performance, même dans des contextes imprévus. En plus de la saisie des demandes, ce système offre un environnement complet pour la validation biologique :
accès aux valeurs de référence et aux antériorités, édition de rapports personnalisés incluant la signature biologique, diffusion rapide des résultats vers les services de soins.
Combiné aux modules de haute disponibilité d’Instrument Manager, Backup SIL devient un pilier de résilience pour les laboratoires.
Parmi les fonctionnalités clés :
• le mirroring en temps réel,
• le basculement automatique en cas de panne,
• les notifications instantanées pour alerter les équipes.
L’ensemble assure une surveillance continue et une continuité de production garantie.
MATERIEL DE LABORATOIRE
Boîtes à déchets en matériaux recyclés

Le secteur de la santé est l’un des plus grands consommateurs de plastiques à usage unique, et ce, pour de bonnes raisons : l’hygiène, la sécurité et la fiabilité. Alors comment concilier responsabilité écologique et exigences élevées de sécurité ?
La société Sarstedt, qui utilise déjà des matériaux recyclés notamment dans la conception de portoirs et d’autres consommables, a présenté ses nouvelles boîtes à déchets DASRI REC avec jusqu’à 61 % de matériau recyclé.
Avec jusqu’à 43 % d’économie d’équivalent CO2 par rapport à une boîte à déchets composée à 100 % de matériaux neufs, la boîte à déchets REC offre une solution plus respectueuse de l’environnement pour l’élimination des objets tranchants et piquants dans le secteur de la santé.
MYCOLOGIE
La précision de la PCR pour le diagnostic fongique
La société Sobioda, qui développe et distribue des réactifs et des systèmes pour les laboratoires de biologie médicale et pour les laboratoires de recherche et d’enseignement, a présenté la gamme de PCR fongique d’IMMY lors de l’édition 2025 de la RICAI.
Adaptable sur la plupart des automates du marché, la gamme IMMY MDx se décline en plusieurs coffrets de qPCR (PCR quantitative) :
• AurisID : spécifiquement conçu pour la détection de Candida auris, ce kit permet la détection du pathogène à partir de sérum, plasma, culture et d’écouvillons de surveillance.
• CandID : ce kit multiplex permet la détection et la différenciation simultanée de 6 espèces de Candida.
• PneumID : dédié à la détection de Pneumocystis jirovecci, ce kit inclus un contrôle interne endogène permettant l’évaluation de la qualité des échantillons.
Ne nécessitant pas de culture, ces kits offrent un gain de temps pour le laboratoire avec un résultat en 45 minutes après extraction.
Tous les kits contiennent également un contrôle interne d’extraction pour l’évaluation de l’efficacité de l’extraction des acides
nucléiques.
En distribuant les solutions IMMY, Sobioda renforce son expertise dans le diagnostic des infections fongiques invasives, en complétant son offre incluant déjà le dosage (1→3)-β-D-glucane.

L’IA d’Owkin capable de dépister les mutations germinales BRCA1/2
Nouvel exemple de la place croissante de l’IA dans les stratégies de diagnostic et de médecine personnalisée, Owkin a présenté de nouveaux résultats internationaux autour de BRCAura, son outil d’IA capable de dépister les mutations germinales BRCA1/2 (anomalies génétiques héréditaires augmentant fortement le risque de cancer du sein et de l’ovaire) directement à partir de lames de pathologie numérisées. Une avancée qui pourrait transformer le dépistage du cancer du sein.
Owkin est une start-up et licorne française, créée en 2016 à Paris, spécialisée en biotechnologies, en informatique médicale et dans l’IA au service de la médecine. Son système BRCAura a démontré des performances solides présentées à l’ESMO 2025 :
• une aire sous la courbe (AUC) de 80 %, indicateur clé de la capacité à distinguer les patientes mutées des non mutées, essentiel pour un dépistage fiable ;
• la possibilité d’écarter environ 40 % des patientes peu susceptibles d’être mutées avec une sensibilité de 93 % ;
• une robustesse confirmée sur plusieurs cohortes internationales.
Ces résultats ouvrent la voie à un dépistage BRCA plus rapide, plus standardisé et plus accessible, en rapprochant pathologie et génomique grâce à l’IA.
BRCAura a été développé à partir de la cohorte PortrAIt, un consortium français majeur dédié à la pathologie numérique (France 2030, France Relance, Next Generation EU) réunissant notamment Gustave Roussy, le Centre Léon Bérard, Unicancer, Tribun Health et Cypath, puis renforcé par une collaboration avec AstraZeneca.
La Fondation Gates mise sur Chembio pour la prééclampsie
Chembio Diagnostic Systems, filiale de Biosynex, entreprise leader dans le domaine du diagnostic Point of Care (POC), a reçu une subvention de 0,5 million de dollars de la Gates Foundation pour le développement d’un test rapide (POC) visant à prédire le risque de prééclampsie chez les femmes enceintes présentant des symptômes compatibles avec cette pathologie.
Depuis plus de 10 ans, des biomarqueurs tels que le PlGF et le sFlt-1 ont confirmé leur valeur pour prédire l’apparition et l’évolution de la prééclampsie chez les femmes présentant des symptômes suspects. Ces biomarqueurs ont montré une forte valeur prédictive négative permettant un suivi ambulatoire sécurisé et sont mesurés en routine dans certains services d’obstétrique des pays à revenu élevé afin d’améliorer et de sécuriser la prise en charge des femmes à risque.
Chembio prévoit de commercialiser un test rapide (lateral flow) simple et peu coûteux pour aider à catégoriser les femmes enceintes présentant des symptômes compatibles avec la prééclampsie. Le test nécessite une goutte de sang (20 microlitres) et le résultat est disponible en moins de 20 minutes. Il détecte le sFlt-1, qui a une forte valeur prédictive pour la prééclampsie. Le résultat peut être lu visuellement ou à l’aide d’un lecteur portable. Ce dispositif a vocation à avoir un impact médico-économique majeur, car une catégorisation optimale favorisera la prise en charge des patientes à risque et permettra également d’éviter des hospitalisations inutiles ainsi que des transferts vers des centres de référence. Il cible principalement les pays à revenu faible et intermédiaire.
Biosynex
Chembio Diagnostic Systems
VIE DES SOCIÉTÉS
En Carta Diagnostics encouragé par la FDA pour son test EC Pocket Lyme
En Carta Diagnostics, start-up deeptech française qui développe des kits de diagnostic moléculaire rapide Point-of-Need, a obtenu la désignation Breakthrough Device (BDD) de la FDA américaine de son test EC Pocket Lyme, destiné à la détection précoce de la bactérie Borrelia, responsable de la maladie de Lyme.
EC Pocket Lyme est un test de diagnostic moléculaire à lecture visuelle immédiate. Il est conçu pour détecter directement la bactérie Borrelia dans le liquide interstitiel de la peau, prélevé sur des personnes présentant des piqûres de tiques ou un érythème migrant. Le test se présente sous forme d’une cassette à usage unique, conçue pour allier précision, prix accessible et facilité d’utilisation, permettant un déploiement à grande échelle. Les résultats sont destinés à aider au diagnostic précoce d’une infection par la bactérie Borrelia.
Cette désignation BDD est réservée aux technologies qui ont montré leur potentiel à fournir un diagnostic ou un traitement plus efficace pour des maladies graves ou invalidantes. Grâce à cette désignation, En Carta Diagnostics bénéficiera d’un examen prioritaire et d’échanges renforcés avec les experts et la direction de la FDA. Cela permettra de soutenir les étapes réglementaires menant à une mise sur le marché plus maitrisée aux États-Unis.
« Cette désignation constitue également une validation externe forte de la qualité, de la robustesse et de la pertinence clinique de notre plateforme », souligne le Dr Margot Karlikow, co-fondatrice et CTO d’En Carta Diagnostics.
La maladie de Lyme est l’une des maladies infectieuses les plus difficiles à diagnostiquer à un stade précoce. Son diagnostic repose sur la détection d’un érythème migrant qui peut passer inaperçu, et sur la détection d’anticorps qui mettent entre 5 à 6 semaines à se développer.
Le test EC Pocket Lyme répond à cette absence de diagnostic précoce grâce à son système de prélèvement à micro-aiguilles qui recueille le liquide interstitiel directement au niveau de la piqûre de tique et grâce à son test de diagnostic moléculaire portable capable de détecter l’ADN des bactéries responsables avant l’apparition de la réponse immunitaire.
S’appuyant sur plus de 10 ans de recherches, la plateforme EC Pocket Lyme exploite une technologie basée sur les aptamères, qui permet une liaison haute affinité et haute spécificité avec des cibles prédéfinies. Ces « signatures » moléculaires peuvent être programmées pour détecter un vaste éventail de maladies génétiques, de pathogènes et de pathologies vétérinaires, ouvrant la voie à de nombreuses applications au-delà de la maladie de Lyme dans le futur.
Dépistage du cancer du col de l’utérus chez les personnes immunodéprimées
La HAS a publié des recommandations spécifiques pour le dépistage du cancer du col de l’utérus chez les femmes immunodéprimées (hors VIH). Cette population présente un risque 3 à 5 fois supérieur de développer des lésions précancéreuses et des cancers invasifs, en raison d’une clairance virale altérée et d’une réponse immunitaire diminuée.
La prévention primaire des infections génitales à HPV repose avant tout sur la vaccination universelle. Cependant, cette vaccination ne protège pas contre la totalité des types potentiellement oncogènes de HPV et la durée de la protection conférée par ces vaccins n’est pas clairement établie, en particulier dans les populations immunodéprimées. Aussi, la vaccination contre le virus HPV n’exempte en aucun cas du dépistage du CCU et d’un suivi gynécologique régulier.
Ainsi, au terme de son évaluation, la HAS a recommandé un dépistage plus rapproché du cancer du col de l’utérus, pour les personnes immunodéprimées suivantes :
• atteintes de déficit immunitaire primitif ou congénital,
• greffées par cellules souches hématopoïétiques allogéniques,
• atteintes de lupus systémique (traitées ou non),
• sous traitement immunosuppresseur depuis au moins un an,
• et toute personne en situation d’immunodépression sévère.
Les intervalles recommandés pour le dépistage pour les personnes immunodéprimées précitées sont les suivants :
• de 25 à 29 ans, la réalisation d’une cytologie annuelle est recommandée,
• de 30 à 65 ans, un premier test HPV est à réaliser à 30 ans, puis tous les 3 ans si les résultats sont négatifs,
• à partir de 65 ans, la poursuite ou l’arrêt du dépistage du CCU devra être décidé selon le résultat du dernier test HPV et en tenant compte des antécédents médicaux.
Modalités de mise en œuvre
Le prélèvement cervical peut être réalisé tel qu’en population générale immunocompétente, par un gynécologue, un médecin généraliste ou une sage-femme et également en laboratoire de biologie sur prescription médicale. Ce sera l’occasion de réaliser ou d’orienter vers le suivi gynécologique médical requis en cas d’immunosuppression. En cas de résultat anormal de dépistage, le suivi, l’orientation et/ou la prise en charge des patientes doivent être assurés par les professionnels de santé.
Enfin, l’auto-prélèvement est une alternative au prélèvement cervical par un professionnel de santé pour la réalisation d’un test HPV pour les femmes à partir de 30 ans, non dépistées ou insuffisamment dépistées selon le rythme recommandé, ou dans le cas particulier d’une mobilité réduite (personnes atteintes de sclérose en plaques par exemple).
« Les Biologistes Médicaux » renouvellent leur équipe
Réunis en Assemblée Générale, les adhérents du syndicat « Les Biologistes Médicaux » ont procédé à l’élection de leur nouveau conseil d’administration pour un mandat de 3 ans. L’équipe élue à l’unanimité et menée par le Dr Lionel Barrand, a reçu un mandat clair pour défendre une biologie médicale d’excellence, ancrée dans le parcours de soins et l’innovation.
Convaincus que le patient est unique, « Les Biologistes Médicaux » intègrent des représentants du secteur public, privé, et de l’internat au sein de leurs instances dirigeantes. « Face aux enjeux de santé publique, l’opposition public/privé est dépassée. Qu’il/elle exerce en CHU, CH ou laboratoire de ville, le/la biologiste médical(e) partage la même expertise. »
Afin de renforcer le positionnement du biologiste médical et de porter des messages de manière unie, le syndicat confirme son engagement moteur au sein de la nouvelle Fédération de la Biologie Médicale, à travers deux membres nommés au sein du Conseil Exécutif : le Dr Morgane Moulis et le Dr Lionel Barrand.
Composition du nouveau Bureau National :
• Président : Dr Lionel Barrand
• Vice-Président (Libéral) : Dr Morgane Moulis
• Vice-Président (Hospitalier) : Dr Eric Guiheneuf
• Vice-Président (Internat) : M. Vincent Guillet
• Secrétaire Général : Dr Pierre-Adrien Bihl
• Secrétaire Général Adjoint : Dr Matthieu Barthélémy
• Trésorier : Dr Nicolas Germain
• Autres membres du bureau : Charles Awoussi, Marouan Bennani, Kévin Cassinari, Stéphanie David, Hervé Fontanet, Lucien Hemar, Alexandre Janel, Kim Nguyen, Stéphanie Haim, Alexis Guérin, Hugo Langris, Patti Liccardo, Guillaume Pax, Laurence Pellegrina, Sophie Perron-Rihaoui, James Kasprzak, Walid Sabeur, Rayan Sater, Paloma Siméon.
Le mot du Président : « Nous remercions nos confrères pour leur confiance renouvelée. Ces trois prochaines années seront décisives. Avec cette équipe élargie, nous avons enfin les armes pour défendre notre modèle : une biologie de proximité, d’expertise et d’innovation, au cœur du système de santé et au service des patients. »
Covid-19 : enfin des marqueurs prédictifs de la gravité de la maladie ?
Une étude de l’Inserm et de l’Université Paris Cité, promue par l’AP-HP et financée en particulier par la Fondation pour la Recherche Médicale et l’ANRS MIE, est née d’un effort collectif pendant les premiers mois de la pandémie de la Covid-19. Elle change la donne en proposant un nouvel outil prédictif capable d’informer des risques de chaque patient grâce à une simple prise de sang. À l’origine de cet outil, la découverte par l’équipe d’Olivia Lenoir et Pierre-Louis Tharaux, chercheurs Inserm, en collaboration avec le consortium Corimuno-19, de marqueurs biologiques associés à une plus forte mortalité à 3 mois des patients hospitalisés pour une pneumonie Covid-19, même peu sévère.
Les chercheurs ont étudié 196 patients admis dans 15 hôpitaux pour une pneumonie modérée à sévère. Des échantillons cliniques ont été récoltés et 41 médiateurs immunitaires et marqueurs de lésions rénales, endothéliales et vasculaires ont été mesurés dans le sang des patients dans les 48 heures suivant leur hospitalisation. Les patients ont été suivis sur 3 mois afin de caractériser précisément l’évolution de leur pathologie. Les chercheurs trouvent ainsi que l’âge au moment de l’inclusion au début de l’étude et 14 variables biologiques (dont 11 protéines) sont indépendamment associés au risque de décès dans les 90 jours.
Parmi ceux-ci, deux marqueurs rénaux (KIM-1 ou kidney injury molecule-1 et LCN2 ou Lipocalin-2) et un marqueur anti-inflammatoire (l’interleukine 10), se sont montrés particulièrement prédictifs de la mortalité. Les concentrations plasmatiques de ces trois marqueurs, mesurées par une simple prise de sang, combinées à l’âge des patients, permettent d’identifier les patients qui sont 2 à 3 fois plus à risque de complications mortelles et ainsi d’élaborer un nouveau score de gravité de la maladie appelé « Corimuno-Score ». Conçu grâce à un modèle statistique multivarié qui prend en compte une grande quantité de facteurs confondants, ce dernier apporte une puissance prédictive maximale rivalisant avec ou surpassant la plupart des tests de laboratoire existants et les prédicteurs déjà en place fondés sur des données cliniques ou sur l’imagerie et souvent bien plus complexes. Ces résultats sont répliqués et validés dans une cohorte indépendante comprenant 105 individus.
Les travaux suggèrent ainsi que le rein est un organe sentinelle négligé dans la pneumonie à SARS-CoV-2 et qui devrait être davantage pris en compte dans les futures études, ne se limitant pas au coronavirus. Ces résultats amènent à reconsidérer les dialogues inter-organes dans les sepsis en général, et en particulier viraux. Les marqueurs identifiés auraient potentiellement un intérêt prédictif dans l’évolution d’autres maladies infectieuses graves, notamment les pneumopathies virales comme la grippe.
LENOIR O et al., Levels of circulating kidney injury markers and IL-10 identify non-critically ill patients with COVID-19 at risk of death, JCI Insight, 2026; 11(2):e198244, doi:10.1172/jci.insight.198244.
Une nouvelle classe de molécule contre les S. pneumoniae résistants
En France, une équipe de chercheurs issue de Chimie ParisTech (PSL) et de l’Institut Pasteur (Université Paris Cité) a mis au point une nouvelle classe de molécules aptes à éliminer la bactérie Streptococcus pneumoniae, ou pneumocoque. Ces molécules innovantes, appelées « aptamères modifiés au ruthénium », ouvrent une perspective inédite contre cette bactérie, souvent résistante aux traitements antimicrobiens classiques.
Ce projet est le fruit de la collaboration entre Marcel Hollenstein (Institut Pasteur), Gilles Gasser (Chimie ParisTech-PSL) et Mélanie Hamon (Institut Pasteur). Ensemble, ils ont transformé des aptamères – de courts fragments d’ADN capables de cibler des molécules précises – en y intégrant des complexes chimiques de ruthénium polypyridyle. Ces modifications leur confèrent la capacité de cibler spécifiquement Streptococcus pneumoniae et de le détruire, une avancée cruciale face à l’impact potentiellement durable du pneumocoque sur les cellules.
La photothérapie : une approche originale
Les complexes de ruthénium, déjà reconnus pour leur activité anticancéreuse in vitro, contiennent un atome métallique et sont désormais explorés pour combattre les infections bactériennes. Leur particularité : agir comme photosensibilisateurs. Une fois activés par la lumière, ils deviennent toxiques pour les bactéries, permettant leur destruction ciblée. Cette technique, la photothérapie, est déjà employée contre certains cancers et repose sur l’activation lumineuse d’une molécule initialement inoffensive.
L’équipe a ainsi développé des aptamères thérapeutiques conférant une grande spécificité au traitement, démontrant que cette stratégie pourrait être utilisée pour contrer la résistance aux antimicrobiens. Après avoir équipé des nucléotides de différents complexes de ruthénium, ils ont prouvé que les enzymes de synthèse de l’ADN pouvaient assembler ces molécules en oligonucléotides, dont certains présentent une forte affinité pour Streptococcus pneumoniae.
Après sept années de recherches, ces résultats montrent qu’il est possible de créer des aptamères puissants contre des cibles bactériennes entières grâce à des nucléotides modifiés. Cette avancée ouvre la voie à de nouvelles stratégies pour lutter contre la résistance aux antimicrobiens, enjeu majeur de santé publique.
FLAMME M et al., Selection of Ruthenium Polypyridyl Complex-Modified Aptamers for Photodynamic Therapy against Streptococcus Pneumonia, J Am Chem Soc, 2025; 147(47): 43612–43628
NOxForum : un congrès pionnier pour une urgence émergente
Les 26 et 27 mars 2026, se tiendra le Congrès NOxForum au Conseil Régional des Hauts de France, à Lille. Porté par le réseau Protoside, ce congrès vise à fédérer tous les acteurs impliqués dans la prévention et la prise en charge des intoxications au protoxyde d’azote, en favorisant les échanges entre professionnels de santé, chercheurs, institutions et associations, pour améliorer la coordination, renforcer les connaissances et impulser des actions concrètes à l’échelle nationale.
Au Programme : plénières et mises à jour des connaissances, tables rondes interactives et présentations de cas, espace partenaires et échanges, restitution des données du réseau Protoside, ateliers participatifs sur les outils de prévention.
Ce congrès s’adresse aux professionnels de santé hospitalier, de ville ou paramédicaux, ainsi qu’aux associations et pouvoirs publics, juristes, avocats…
Le mot d’ordre des présidents du Congrès, le Dr Cécile Bossaert (membre SFMU) et Guillaume Grzych (membre SFBC) :
« Ensemble, retrouvons-nous pour parler d’une même voix de la réalité du Protoxyde d’Azote ! »
Journée scientifique « Hématologie et Environnement »

Peut-on encore appréhender les maladies du sang sans intégrer les déterminants environnementaux qui les influencent ?
Dans un contexte marqué par le changement climatique, l’évolution des expositions environnementales et l’émergence de nouvelles menaces sanitaires, il devient essentiel pour la communauté hématologique de s’interroger sur les liens entre l’environnement et les pathologies du sang.
C’est pourquoi une journée scientifique « Hématologie et Environnement » est organisée à l’Institut Imagine de l’Hôpital Necker Enfants malades, le 17 avril 2026, au nom du groupe Hematogreen, par le Dr Bérénice Schell.
Cette journée vise à éclairer ces enjeux à travers des interventions d’experts et des approches pluridisciplinaires. Les détails du programme ainsi que les modalités d’inscription sont disponibles en suivant le QRCode ci-contre.
Journée scientifique « Hématologie et Environnement »
Pour leur 68e édition, les JIB se réinventent !
Après une année blanche, le Syndicat des Biologistes (SDBio) propose à nouveau aux biologistes de «venir à la rencontre de l’innovation en biologie médicale» : les JIB 2026 se tiendront les 19 et 20 novembre 2026 à Paris.
Nouvelle identité, nouveau logo, et nouveau lieu emblématique pour marquer cette transformation : le Centre des Congrès de La Villette, à la Cité des Sciences et de l’Industrie de Paris, accueillera cette nouvelle édition. Celle-ci incarnera la volonté des JIB d’allier renouveau et continuité, en préservant l’excellence scientifique et la dynamique professionnelle qui font leur renommée.
Au programme : conférences, échanges, innovations et moments forts, pour rassembler la grande communauté de la biologie autour d’un objectif commun : imaginer et bâtir la biologie de demain, portée par les avancées de l’AI.
Les Journées de l’Innovation en Biologie éclairent la discipline de biologie avec des conférences scientifiques de haut niveau, des tables rondes engagées sur la profession, des rencontres inspirantes avec les partenaires, la présentation de matériel innovant et de nombreuses opportunités d’échange passionnant.
Pour François Blanchecotte, président du SDBio : « S’il est une profession au cœur de l’innovation en santé portée par l’intelligence artificielle, c’est bien la nôtre. Biologistes, avec nos partenaires, nous sommes aux avant-postes des transformations techniques profondes qui traversent le système de santé. C’est cette dynamique que nous vous invitons à venir découvrir lors des JIB 2026, qui reviennent réinventées, porteuses d’un nouvel élan pour la communauté de la biologie médicale. »
JIB 2026
Syndicat des Biologistes, SDBio
Le SNBH prend le relais des Journées en biologie d’urgence « Alain Feuillu »
À l’occasion des 8es JFBM, le SNBH a annoncé reprendre l’organisation du Symposium « Alain Feuillu » en biologie d’urgence, rebaptisé désormais Symposium International de Biologie d’Urgence (SIBU). Après une dernière édition à Saint-Malo en 2024, les Drs Michel Vaubourdolle et Christian Aussel souhaitaient passer le relais à une nouvelle équipe dynamique.
Raphaël Bérenger, président du SNBH, a souligné l’importance et l’honneur de perpétuer ce congrès, reconnu et salué par la profession pour la vitalité de ses échanges scientifiques.
Les équipes du SNBH et des JFBM ont décidé de relever le défi les 10 et 11 juin 2027 au Centre des congrès de Nîmes, et prévoit de conserver la fréquence d’origine d’un colloque un an sur deux.
Le comité d’organisation réunit Raphaël Bérenger (président du SNBH et des JFBM), Vincent Estève (vice-président du SNBH), David Guenet (trésorier du SNBH), et Philippe Souquières (PSO4Events), tous impliqués dans la réussite des JFBM. Avec ce renouveau, le SIBU veut s’affirmer comme le futur événement incontournable pour la biologie d’urgence.
Symposium International de Biologie d’Urgence, SIBU
MANIFESTATIONS
2026
– 10-11 mars Forum – Labo 2026 – LYON – www.forumlabo.com
– 12 mars – 2e Journée IA & Pathologie – PARIS – www.jiap-sfp.org/
– 25-26 mars – Tech 4 Health – PARIS – www.tech-4health.com/fr
– 25-27 mars – 46e Congrès de la Société Française d’Hématologie (SFH) – PARIS – https://sfh.hematologie.net/congres
– 26 -27 mars – Congrès Protoside – LILLE – https://noxforum.protoside.com/
– 17 avril – Journée scientifique « Hématologie et Environnement » – PARIS – https://framaforms.org/inscription-a-la-journee-hematologie-et-environnement-1759590457
– 21-24 avril – 21e Congrès Francophone d’Allergologie – PARIS – https://register.congres-allergologie.com/
– 19-21 mai – Santexpo 2026 – PARIS – https://www.santexpo.com/
– 28-29 mai – Biomed-J 2026 – PARIS – www.congres-biomedj.fr
– 3-5 juin – 36ème Congrès de la SF2H – LILLE – https://www.sf2h.net/congres/36eme-congres-sf2h-lille-2026.html
– 3-5 juin – Urgences 2026 – PARIS – https://urgences-lecongres.org/
– 4-5 juin – 13e Colloque du GEAI (Groupe d’Étude de l’Auto-Immunité) – PARIS – www.alphavisa.com/geai/2026/index.php
– 30 septembre-2 octobre – Congrès de la Société Française de Thrombose et d’Hémostase (SFTH) – NÎMES – https://www.congres-hemostase.com/
– 7-9 octobre – 21e congrès annuel de la Société Française de Microbiologie (SFM) – LYON – www.alphavisa.com/sfm/2026/fr/
– 14-16 octobre – 9e JFBM – LE HAVRE – https://www.jfbm2025.fr
– 18-20 novembre – XVIe congrès de la SFVTT (Société Française de Vigilance et de Thérapeutique Transfusionnelle) – TOULOUSE – https://www.sfvtt.org/congre/xvi-eme-congres-national-de-la-societe-francaise-de-vigilace-et-de-therapeutique-transfusionnelle
– 19-20 novembre – Journées Internationales de Biologie (JIB) – PARIS – https://lesjib.org/
– 25-27 novembre – 1st Mediterranean Meeting on Flow Cytometry – GRENADE (ESPAGNE) – https://www.alphavisa.com/cytometry/2026/index.php
2027
– 10-11 juin – Symposium International de Biologie d’Urgence (SIBU) – NIMES – https://sibu2027.com/
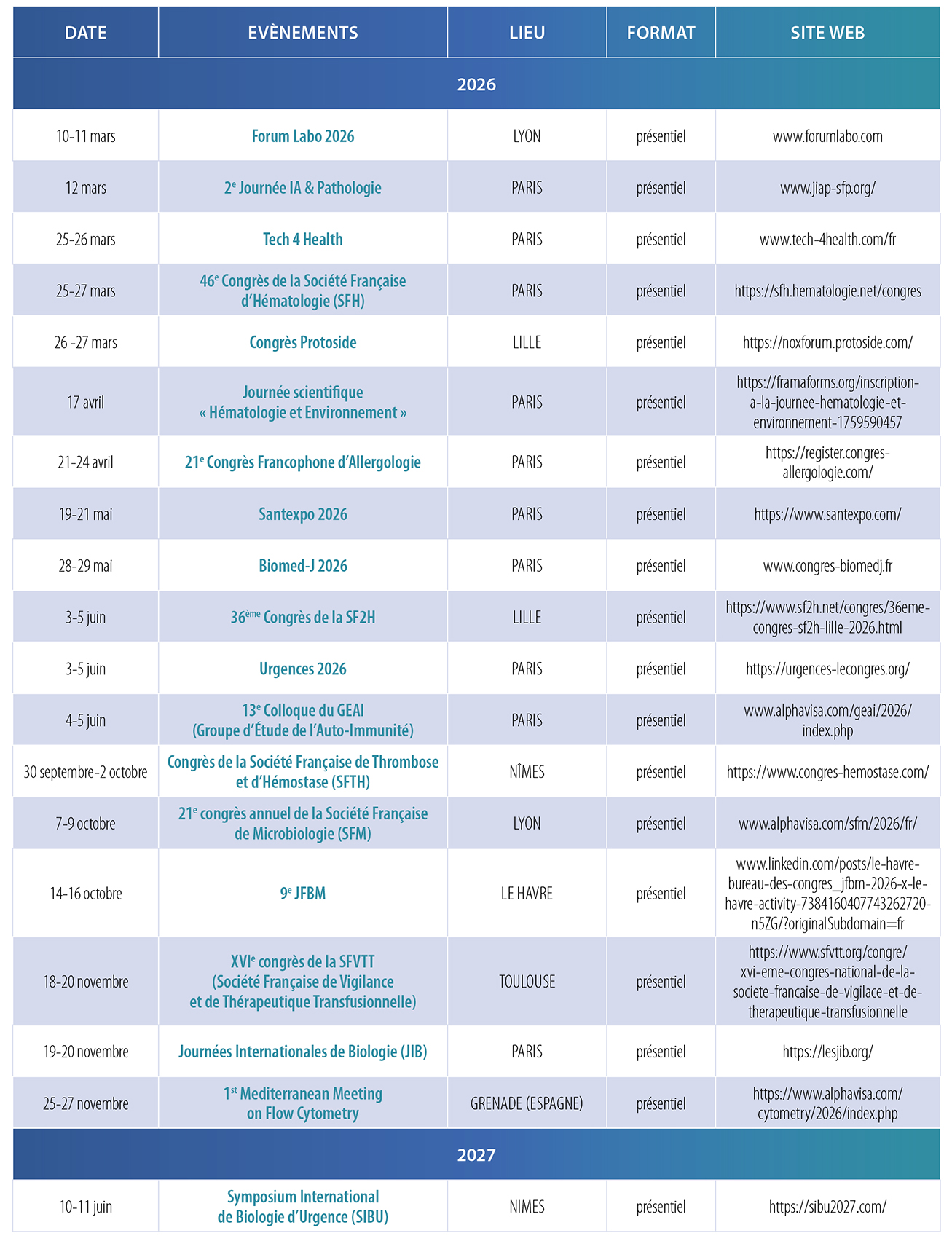
Retrouvez dans Spectra Diagnostic N°42 :
BOURSE & BIOTECHS
Le Groupe biopharmaceutique français IPSEN a le vent en poupe
Gizem YILDIRIM, Constance DEPEIGNE, Agathe MORET, Chaima ESSAOUI, Arsia AMIR-ASLANI
BIOTECHNOLOGIES
L’intelligence Artificielle en Chine : Quelles sont les composantes clés du modèle chinois ?
Félix VIDAL, Philippe LE, Arsia AMIR-ASLANI
BIOACTEUR
Création de la Fédération de la biologie médicale :
La biologie médicale de ville s’organise pour affronter les futurs défis de la profession
CAS BIOCLINIQUES
Cas bioclinique : quiz
Bruno BAUDIN
MISE À JOUR DES CONNAISSANCES
Recherche des antigènes urinaires de Legionella pneumophila :
limites techniques et impact sur les pratiques pour le diagnostic étiologique d’une pneumonie
Ylhame Kahina SOUAMI
Newsletter Spectra Diagnostic N°41

BIOLOGIE MOLECULAIRE
PCR Multiplex en test unitaire, pour tout laboratoire

Les Laboratoires Nephrotek présenteront à la RICAI les modèles FlashDx-1000-E ainsi que la solution évolutive sSPRT 4T/8T/12T basée sur la technologie propriétaire sSPRT (semi-Solid-Phase-Real-Time-PCR). Chaque test est effectué à partir d’une cartouche micro-fluidique prête à l’emploi.
Possédant une capacité de traitement de 1 à 12 tests simultanément, la gamme FlashDx est parfaitement adaptée à l’EBMD (Urgences) et au laboratoire central, permettant la recherche multiplex d’une dizaine de pathogènes avec un rendu de résultat en moins de 60 minutes.
Les panels disponibles sont :
• SARS-CoV-2
• SARS-CoV-2, VRS, Grippe A et B
• Respiratory panel 1.1 : SARS-CoV-2, VRS, Grippe A et B, MP, BP, MPV, AdV, HRV/HEV, PIV (1,2,3)
• Respiratory panel 2 : PIV (4), SARS-CoV-2 (229E, OC43, NL63, HKU1), Bocavirus, Chlam. P., BP (IS481), BPP (IS1001)
• Arbovirus : Chikungunya, Zika, WNV, YFV, Dengue 1/2/3/4
• SGB : Streptococcus B
• MRSA / SA : Methicillin-resistant Staphylococcus aureus, Staphylococcus aureus
• CRE (Carba) : IMP, VIM, NDM, KPC, OXA
• STI : CT, NG, MG MH UU, TV
ANALYSES
Premier test sanguin pour la maladie d’Alzheimer
L’obtention récente du marquage CE-IVDR pour le test Elecsys® phospho-Tau (181P) Plasma marque une avancée majeure : il s’agit du premier test sanguin d’aide au diagnostic de la maladie d’Alzheimer (MA) à être approuvé en France et en Europe. Cette innovation illustre l’importance croissante des biomarqueurs sanguins, qui rendent la détection précoce des altérations pathologiques typiques de la MA plus accessible et moins invasive, et ouvrent la voie à un véritable changement de paradigme dans la prise en charge de la maladie. Traditionnellement, le diagnostic de la MA repose sur une combinaison de tests d’évaluation cognitive et de diagnostics de confirmation. Cependant, confirmer la maladie nécessite des procédures soit invasives, soit coûteuses et souvent éprouvantes pour les patients : ponction lombaire ou tomographie par émission de positons (TEP).
Elecsys® Phospho Tau (181P) Plasma est un test immunologique quantitatif in vitro pour la détermination de la protéine phosphorylée Tau 181 dans le plasma humain. Ses résultats sont destinés à la détection précoce d’une pathologie amyloïde chez les adultes de 55 80 ans souffrant d’affections subjectives ou de troubles cognitifs non spécifiques (déficit cognitif subjectif) ou ceux suspectés par leur médecin de présenter des troubles cognitifs légers et qui font l’objet d’une évaluation de la MA. Le résultat de ce test doit être considéré comme une aide au diagnostic de la MA, en association avec d’autres informations cliniques.
D’autre part, le test sanguin Elecsys® pTau217, en cours de développement, sera un test immunologique de diagnostic in vitro pour la détermination quantitative de la protéine Phospho-Tau (217P) dans le plasma humain. Il sera destiné à aider à identifier la pathologie amyloïde.
MATERIEL DE LABORATOIRE
Analyses parasitologiques : une solution préanalytique sans mercure

Les infections parasitaires à l’origine de troubles gastro-intestinaux (diarrhées, douleurs abdominales, ballonnements, malabsorption) nécessitent un examen parasitologique fiable et précis. La qualité de ce diagnostic repose sur la préservation de la morphologie des parasites et sur la bonne concentration de l’échantillon dès la phase préanalytique.
Les dernières recommandations ANOFEL/LABAC soulignent l’importance d’utiliser des fixateurs performants tels que le MIF (Merthiolate–Iode–Formol) ou le SAF (Acide acétique–Acétate de sodium–Formol). Aujourd’hui, le SAF s’impose comme la référence sans mercure, particulièrement adaptée aux colorations spécifiques pour la recherche de coccidies en microscopie.
La solution MIF, historiquement utilisée, contient du thiomersal (composé mercuriel) et du formaldéhyde, deux substances dangereuses et strictement réglementées en Europe. Le règlement (UE) 2017/852 et le Code du travail (art. R.4412-66) imposent désormais la substitution des produits à base de mercure dès qu’une alternative existe. Les CDC et l’OMS recommandent d’ailleurs le SAF comme solution de remplacement sûre et conforme.
Launch Diagnostics propose Para-Pak®, une gamme complète de fixateurs et de conservateurs spécialement conçus pour optimiser le transport, l’examen direct et la concentration des échantillons de selles.
• Sans mercure, conforme aux recommandations nationales et internationales
• Excellente préservation morphologique des parasites
• Diagnostic plus fiable, même en cas de délai d’acheminement prolongé
• Large choix de formulations adaptées aux besoins de chaque laboratoire.
Ainsi, les selles émises en dehors du laboratoire sont immédiatement stabilisées, garantissant une observation microscopique optimale et un résultat diagnostique précis et reproductible.
CONTROLE QUALITE
Nouveaux contrôles indépendants d’immunodosages spécialisés
Les contrôles Specialty lmmunoassay Plus représentent la nouvelle génération de contrôles indépendants d’immunodosages spécialisés de la société Bio-Rad. Au format liquide, ils sont intégrés à la solution de gestion des données Unity afin de garantir des résultats fiables à chaque analyse.
Specialty Immunoassay Plus est un contrôle qualité à quatre niveaux, complet et indépendant, conçu pour surveiller la fidélité des immunoanalyses spécialisées. Cette gamme comprend des analytes très demandés et cliniquement pertinents dont 6 nouveaux : procalcitonine (PCT), IL-6, vitamine B12 active, fructosamine, TRAb et TSI.
Ces contrôles améliorés offrent la consolidation de 14 analytes : le menu étendu d’analytes permet de regrouper tous les analytes dans un seul flacon. Les formats liquides InteliQ et Liquichek sont prêts à l’emploi et ne nécessitent donc plus de reconstitution pour gagner en temps de manipulation. Ils offrent les autres avantages suivants :
• Analytes clés pour les immunodosages spécialisés, dont la procalcitonine (PCT) et l’IL-6
• Optimisé pour les analyses conformes au programme de standardisation de la vitamine D (VDSP)
• Stabilité de 30 jours après ouverture du flacon pour la plupart des analytes et de 14 jours pour la PTH intacte
• Configuration « load-and-go » disponible, prêt pour l’automatisation
• S’intègre à la solution de gestion de données de contrôle Unity.
Enfin, ils sont disponibles en plusieurs formats pour répondre aux besoins de chaque laboratoire.

Ascentry x Inlog officialisent leur partenariat stratégique
Ascentry (anciennement BYG4lab), éditeur spécialiste du middleware, et Inlog (SGL & transfusion), éditeur reconnu de solutions SIL, annoncent une collaboration active afin de proposer une offre globale et intégrée.
Ce partenariat vient officialiser une collaboration déjà existante entre les deux sociétés, initiée depuis plusieurs années à travers des projets communs dans des établissements de santé. En structurant cette alliance, les deux entreprises souhaitent désormais accélérer les déploiements, renforcer leur coordination et proposer une offre commune cohérente et performante pour les laboratoires.
David Kalfon, Directeur Général d’Inlog : « Cet accord marque une nouvelle étape qui s’est concrétisée récemment par les Hôpitaux Paris Saint-Joseph Marie-Lannelongue qui ont fait le choix de nos deux solutions respectives pour digitaliser l’ensemble des laboratoires ».
Cyril Verhille, CEO d’Ascentry : « Inlog jouit d’une très bonne réputation non seulement en France mais également dans de nombreux pays. Cet accord est en ligne directe avec notre stratégie d’alliance et d’internationalisation ».
Acteur majeur du secteur de la santé, Ascentry compte 120 collaborateurs et dispose de filiales aux États-Unis et en Finlande. A ce jour, 5 000 solutions Ascentry sont utilisées à travers le monde. L’entreprise est experte en solutions de Data Management dédiées aux LBM, au suivi épidémiologique des établissements et à la prévention des infections associées aux soins.
Inlog est un leader européen dans le domaine de l’informatique transfusionnelle et un acteur majeur sur le marché des SGL (Systèmes de Gestion de Laboratoires). Fondé en 1992, Inlog est l’un des principaux éditeurs français en matière d’informatique médicale pour les LBM, les hôpitaux et les centres de transfusion sanguine.
Sebia accueille Warburg Pincus à son capital pour soutenir ses ambitions
Sebia, acteur spécialisé du diagnostic in vitro et fournisseur mondial de solutions innovantes pour le dépistage et le suivi de certains cancers, maladies métaboliques, génétiques et auto-immunes, est entré en négociations exclusives en vue d’une évolution partielle de son capital, avec le soutien renouvelé de ses actionnaires historiques – Téthys Invest, CVC et La Caisse.
Dans le même temps, Warburg Pincus, société de capital-investissement de premier plan spécialisée dans la Santé, rejoindrait le capital de Sebia en tant qu’actionnaire minoritaire significatif. Cette étape importante dans le développement du groupe témoigne de la volonté de Warburg Pincus d’accompagner des entreprises innovantes du secteur des sciences de la vie à l’échelle mondiale. Warburg Pincus apportera à Sebia son expertise approfondie en santé ainsi que son vaste écosystème international, notamment aux États-Unis.
Fondée en 1967, Sebia connait depuis fin 2017 une croissance exceptionnelle et a significativement élargi son marché au-delà de l’oncologie (notamment le myélome multiple), en se développant dans le diagnostic des troubles métaboliques tels que le diabète, les hémoglobinopathies et les maladies auto-immunes. Ces avancées ont été rendues possibles grâce à plusieurs acquisitions stratégiques aux États-Unis, en Allemagne et en Nouvelle-Zélande – Orgentec, Corgenix, Arotec (2021) et Zeus Scientific (2022). L’inauguration récente d’un nouveau site de production et d’un centre d’excellence de R&D à Lisses (France) illustre le dynamisme et les ambitions de croissance de Sebia. Cette extension renforce les capacités d’innovation du groupe, notamment dans le domaine de la maladie résiduelle du myélome multiple, du sepsis et de l’endométriose, et soutient ses perspectives de développement à long terme.
Les managers et employés de Sebia, représentés par leur PDG Jean-Marc Chermette, demeurent actionnaires à l’issue de cette évolution capitalistique.
« Nous sommes ravis d’accueillir Warburg Pincus aux côtés de nos actionnaires existants, qui réaffirment leur engagement à nos côtés. Cette évolution ouvre une nouvelle étape dans l’histoire de Sebia, portée par une dynamique d’innovation sans précédent et des relais de croissance prometteurs dans plusieurs aires thérapeutiques majeures. Nous nous réjouissons de collaborer avec un partenaire international de référence pour accélérer notre expansion – en particulier aux États-Unis – et renforcer notre position d’acteur mondial du diagnostic de spécialité », déclare Jean-Marc Chermette.
VIE DES SOCIÉTÉS
Valab développe sa stratégie Export et recrute Andreia Moreira
Dans la continuité de son développement à l’international, les équipes de l’éditeur Valab ont été présentes cette année sur les salons européens phares de la biologie médicale : la 17e édition du SPML (Sociedade Portuguesa de Medicina Laboratorial) au Portugal (14-15 avril), l’OGLMKC (Österreichischen Gesellschaft für Laboratoriumsmedizin und Klinische Chemie), salon bisannuel organisé en Autriche (25-27 juin), le congrès DKLM (Deutscher Kongress für Laboratoriumsmedizin) en Allemagne (23-24 Octobre), suivie du SIBIOC (Società Italiana di Biochimica Clinica e Biologia Molecolare Clinica) en Italie (05-07 novembre), puis le salon LABCLIN en Espagne (12-14 novembre).
Ces différentes actions s’inscrivent dans la dynamique européenne de la société, marquée cette année par une première installation au Portugal dans un LBM privé, grâce à un nouveau partenariat avec la société Slice, leader sur le marché portugais et fournisseur du SIL, edeiaLab. Un second laboratoire privé sur le sol autrichien a été également équipé avec Valab, en étroite collaboration avec son partenaire local, Assista. Valab s’ouvre désormais les portes de l’Irlande avec le premier laboratoire privé validant plus de 4 000 dossiers par jour.
Enfin, Valab étend désormais sa présence dans les pays LaTam avec une installation en cours au Chili dans un regroupement de 7 laboratoires, marquant une ouverture à l’international hors Europe.

Andreia Moreira, nouvelle directrice adjointe chez VALAB
Dans ce contexte, la société a créé un poste de directrice adjointe afin de renforcer sa direction et en a confié la responsabilité à Andreia Moreira.
Docteure en bio-informatique, Andreia Moreira possède une solide expérience dans la maîtrise des logiciels destinés aux LBM. Sa connaissance du secteur de la biologie médicale, alliée à son parcours international, sera mise à profit dans les futurs développements de Valab®, qu’ils soient techniques ou internationaux. Grâce à la pratique de cinq langues étrangères (espagnol, catalan, italien, portugais et anglais), Andreia constituera un atout pour la présence de la société en Amérique latine et en Europe.
« Je suis honorée de cette nomination et ravie d’intégrer la direction de Valab. Avec l’équipe, nous avons pour objectif dans les années à venir, de continuer à faire évoluer notre solution Valab®, ses modules ainsi que nos services. Ceci dans le but de maintenir notre leadership sur le territoire français, de consolider les marchés récemment développés, tout en conquérant de nouveaux marchés à l’international, et dans de nouvelles disciplines. La prochaine version, prévue dans les mois à venir, introduira des innovations conférant un caractère polyvalent à notre système expert, lui permettant de s’appliquer à d’autres domaines d’expertise », a déclaré Andreia.
AKO@dom-Picto va être généralisé pour le suivi en ville des patients sous thérapies orales anticancéreuses
Le Comité Technique de l’Innovation en Santé (CTIS) et le Conseil Stratégique de l’Innovation en Santé (CSIS) ont rendu un avis favorable à la généralisation de l’expérimentation des parcours de soins AKO@dom et Picto qui associent infirmiers libéraux, pharmaciens d’officine et médecin traitant pour le suivi et l’accompagnement à domicile des patients sous thérapies orales anticancéreuses.
Depuis 3 ans, ces parcours faisaient l’objet d’une expérimentation dans 15 établissements de la région Grand-Est, dans le cadre du dispositif d’innovation en santé « Article 51 », un cadre expérimental introduit par la LFSS 2018 visant à encourager, accompagner et accélérer le déploiement de nouvelles organisations et de nouveaux modes de financement en santé.
Le projet visait à expérimenter un accompagnement humain et numérique personnalisé des patients atteints de cancer, au moment de la prescription d’une thérapie orale et/ou d’une immunothérapie. C’est la seule des 156 expérimentations dans le cadre de l’article 51 à être co-portée par une association de patients. Plus de 2000 patients ont pu bénéficier de ces
parcours depuis 2022.
Une plateforme numérique pour un suivi réactif
Les parcours AKO@dom et Picto associent à l’humain l’outil numérique. Une plateforme unique, mise à disposition par Continuum + (intégrée à Cureety), permet aux oncologues et aux infirmiers de coordination hospitalière de suivre en temps réel le contenu des visites infirmières et les comptes rendus des pharmaciens d’officine. La plateforme permet ainsi une grande réactivité dans la gestion des alertes.
Les résultats de l’évaluation, présentés dans l’avis du CTIS, ont été très positifs selon toutes les parties : les patients se sentent rassurés, écoutés et moins isolés. 85% des professionnels de santé se disent convaincus tant de l’amélioration de la prise en charge que du renforcement du lien entre les professionnels de ville et hospitaliers. La communication en temps réel évite des allers-retours inutiles des patients à l’hôpital. L’observance des traitements après 6 mois est de 70 % (versus 60 % dans un groupe témoin). Les évènements indésirables sont mieux gérés : détection précoce des effets indésirables, échanges en temps réel avec le pharmacien d’officine ou l’IDE libéral sur la plateforme pour ajuster les traitements sans attendre les consultations de suivi. La durée des hospitalisations pour des évènements indésirables était réduite à 5 jours (versus 13 jours pour les cas témoins). Les pharmaciens se disent légitimés et mieux armés pour prendre en charge les malades atteints de cancer et constatent que la relation avec les patients en sort renforcée. Enfin, le déploiement de ces parcours a permis une transformation de la relation ville-hôpital, un décloisonnement des prises en charges et a su mobiliser un nombre conséquent de professionnels de santé en ville.
Surveillance des cancers colorectaux réséqués : moins d’examens, sans perte de chances
Une étude académique française de grande ampleur, PRODIGE-13, menée par la Fédération Francophone de Cancérologie Digestive (FFCD), a démontré qu’il était possible de simplifier les modalités de la surveillance après chirurgie des cancers colorectaux sans compromettre la survie des patients, avec des conséquences importantes en pratique.
Conduite par le Pr Côme Lepage (Université de Bourgogne Europe, CHU Dijon) sur 2 009 patients suivis pendant plus de 10 ans dans 120 centres, avec la participation de près de 1000 spécialistes en France et en Belgique, cette étude unique au monde a montré des résultats sans équivoque : ni la surveillance des dosages sanguins répétés (Antigène carcinoembryonnaire, ACE), ni la réalisation de scanners thoraco-abdomino-pelviens annuels n’ont permis d’améliorer la survie après résection curative d’un cancer du côlon par rapport à un suivi simple avec échographies abdominales et radiographies pulmonaires.
En conséquence, l’auteur invite à pratiquer moins d’examens pour plus de bénéfices. Pour les patients, cela implique moins de stress, d’irradiation, ou d’effets secondaires liés aux produits de contraste. Pour le système de santé, cela libère les scanners pour d’autres malades, et la surveillance sera moins coûteuse. Enfin, pour la recherche, cette étude prouve la capacité française à mener des essais académiques de référence ouvrant la voie à d’autres études.
« C’est l’étude de surveillance la plus importante jamais conduite dans le monde. Elle va permettre un changement des pratiques tout en assurant une surveillance optimale » indique le Pr Côme Lepage.
Fédération Francophone de Cancérologie
L’aspirine délétère à long terme chez les patients sous anticoagulants ?
Chez les patients cumulant une maladie coronaire chronique et la nécessité d’un traitement anticoagulant, une question importante se pose au quotidien : faut-il maintenir l’aspirine en plus du traitement anticoagulant à long terme ? Cette combinaison pourrait renforcer la prévention des caillots mais aussi augmenter le risque de saignements. C’est pour répondre à cette question que l’étude nationale AQUATIC a été menée par des chercheurs français hospitaliers.
Portée par le Pr Martine Gilard, Cardiologue au CHU de Brest, le Pr Gilles Lemesle, Cardiologue au CHU de Lille et le Pr Guillaume Cayla, Cardiologue au CHU de Nîmes, l’étude a pu compter sur l’appui notamment des trois grands réseaux académiques français de recherche en cardiologie : le réseau F.A.C.T, le groupe A.C.T.I.O.N et la Société Française de Cardiologie.
La conduite méthodologique et statistique de l’étude a été assurée par le Pr Eric Vicaut de l’Unité de Recherche Clinique Lariboisière–Saint-Louis à Paris.
Menée dans 51 centres de cardiologie en France, l’étude a inclus 872 patients atteints d’une maladie coronaire chronique, à haut risque de récidive, et traités par anticoagulants. Le suivi médian a été de deux ans. Elle s’est arrêtée de manière anticipée car les résultats ont indiqué que l’ajout d’aspirine n’offrait aucune protection supplémentaire sur le risque de récidive par rapport au traitement anticoagulant seul. En revanche, une augmentation significative des hémorragies a été observée avec l’aspirine. De manière importante, le pronostic des
patients sans aspirine était significativement meilleur.
Les résultats de l’étude AQUATIC sont clairs et pourraient modifier les prochaines recommandations internationales de cardiologie en notifiant que pour les patients coronariens chroniques, y compris pour ceux qui ont un risque élevé, l’aspirine ne doit pas être prescrite à long terme en plus du traitement anticoagulant lorsque celui-ci est nécessaire notamment pour une fibrillation atriale. L’application en pratique quotidienne des résultats de cette étude vont permettre d’améliorer le pronostic de ces patients coronariens sous anticoagulant. Cette étude illustre également la réussite d’une collaboration originale entre trois CHU français dans le cadre des projets nationaux hospitaliers de recherche clinique (PHRC).
LEMESLE G et al., Aspirin in Patients with Chronic Coronary Syndrome Receiving Oral Anticoagulation, N Engl J Med, 2025; 393:1578-1588, doi:10.1056/NEJMoa2507532
Une piste prometteuse pour augmenter l’efficacité des antibiotiques
Des chercheurs de l’Institut Pasteur, en collaboration avec l’Inserm, le CNRS et l’Université Paris Cité, ont élucidé le mécanisme d’entrée des aminosides, une classe d’antibiotiques très utilisée, dans les bactéries telles qu’Escherichia coli, Pseudomonas aeruginosa ou Staphylococcus aureus. Jusqu’alors, le mode de pénétration de ces antibiotiques restait inconnu, certaines hypothèses suggérant une traversée passive de la membrane bactérienne. Les scientifiques ont démontré que les aminosides empruntent les transporteurs des sucres, véritables « portes d’entrée » pour des molécules comme le glucose ou le fructose, pour franchir la double membrane des bactéries pathogènes.
Cette découverte, rendue possible grâce à l’étude de la bactérie Vibrio cholerae, a permis de constater l’existence d’une corrélation entre l’efficacité des aminosides et la présence de transporteurs de sucres. En poursuivant leurs recherches sur E. coli, les scientifiques ont observé, grâce à la fluorescence, que les aminosides pénètrent activement dans les bactéries via ces transporteurs. Ce mode de transport n’avait encore jamais été mis en évidence pour des antibiotiques.
Conscients de la plasticité de ces transporteurs, dont le nombre fluctue selon le type de sucre disponible, les chercheurs ont voulu augmenter leur quantité dans les bactéries afin d’améliorer la perméabilité aux aminosides. Sur 200 composés testés, l’uridine s’est révélée capable de doubler le nombre de transporteurs de sucres dans les bactéries E. coli, y compris les plus résistantes. Cette augmentation de transporteurs a permis de multiplier par dix la sensibilité des bactéries aux aminosides, et de rendre perméables des souches résistantes voire multi-résistantes. Des effets similaires ont été observés avec d’autres espèces bactériennes.
Les perspectives sont majeures : l’administration d’uridine pourrait réduire les doses d’antibiotiques nécessaires, limitant ainsi les risques de résistance et les effets secondaires, notamment la toxicité des aminosides pour l’oreille interne ou les reins. L’uridine, déjà utilisée en clinique et jugée non toxique chez l’humain, ouvre la voie à des essais cliniques accélérés et à la conception de molécules innovantes. Les chercheurs envisagent également de « greffer » l’uridine à divers antibiotiques pour faciliter leur pénétration dans les bactéries résistantes.
LANG M et al., Uridine as a potentiator of aminoglycosides through activation of carbohydrate transporters, Science Advances, 2025; 11(36):eadw7630, doi:10.1126/sciadv.adw7630
MANIFESTATIONS
2025
– 3-5 décembre – Paris Santé Femmes – PARIS – https://paris-sante-femmes.fr
– 11-12 décembre – SFTS 2025 – BRUXELLES – https://www.sfts.asso.fr/congres/bienvenue
– mi décembre – 44e Réunion Interdisciplinaire de Chimiothérapie Anti-Infectieuse (RICAI) 2025 – PARIS – https://www.ricai.fr/
2026
– 10-11 mars – Forum Labo 2026 – LYON – www.forumlabo.com
– 12 mars – 2e Journée IA & Pathologie – PARIS – www.alphavisa.com/geai/2026/index.php
– 25-26 mars – Tech 4 Health – PARIS – www.tech-4health.com/fr
– 28-29 mai – Biomed-J 2026 – PARIS – www.congres-biomedj.fr
– 4-5 juin – 13e Colloque du GEAI (Groupe d’Étude de l’Auto-Immunité) – PARIS – www.alphavisa.com/geai/2026/index.php
– 7-9 octobre – 21e congrès annuel de la Société Française de Microbiologie (SFM) – LYON – www.alphavisa.com/sfm/2026/fr/
– 14-16 octobre – 9e JFBM – LE HAVRE – https://snbh.org/
– 19-20 novembre – Journées Internationales de Biologie (JIB) – PARIS – www.jib-innovation.com
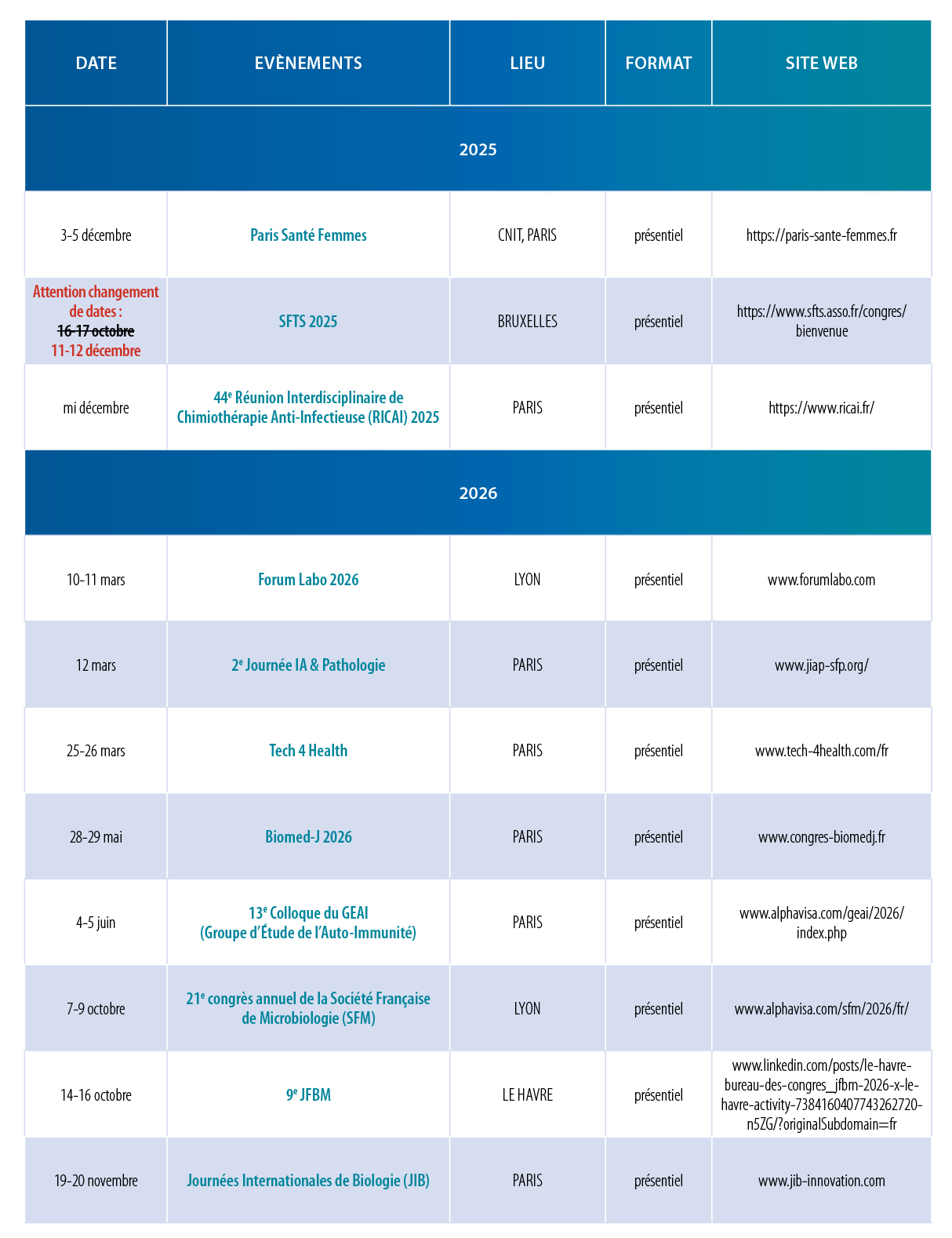
Retrouvez dans Spectra Diagnostic N°41 :
BOURSE & BIOTECHS
Abivax affiche une performance boursière à la GAFAM
Arsia AMIR-ASLANI
BIOTECHNOLOGIES
Pourquoi les biotechs danoises surpassent-elles les françaises ?
Une leçon d’écosystème et de stratégie
Jude Nathanaël P. OUEDRAOGO, Arsia AMIR-ASLANI
BIOTECHNOLOGIES
L’intelligence artificielle aux Etats-Unis : Quels sont les facteurs clés du succès ?
Félix VIDAL, Arsia AMIR-ASLANI
TECHNOLOGIE APPLIQUÉE
Retours d’expérience sur les middlewares de microbiologie – partie 2
Thierry DIEUDONNE
CAS BIOCLINIQUES
Cas bioclinique : quiz
Bruno BAUDIN
CAS BIOCLINIQUES
Dépistage rapide de drogues urinaires aux urgences pédiatriques : à propos d’un cas
Manon GONÇALVES, Charlotte DUMONT, Julie JOURDAN, Laurence MOULY
CAS BIOCLINIQUES
D’un cas de thyroïdite d’Hashimoto à la prise en charge familiale d’un adénocarcinome papillaire
Ylhame Kahina SOUAMI











