

ANALYSEUR
Panels sepsis sur mesure par RT-PCR en 1 heure
Le distributeur indépendant Launch Diagnostics France SAS distribue désormais le fabricant italien Alifax en France, et continue ainsi son expansion dans le domaine de l’antibiorésistance (biologie moléculaire, tests rapides, bandelettes de CMI …).
Fondée en 1988, la société Alifax S.r.l., basée à Trieste en Italie, est spécialisée dans la mise en œuvre de solutions innovantes pour lutter contre l’antibiorésistance. Le nombre de décès par septicémie est en constante évolution dans le monde et une détection précoce est un outil essentiel dans la bonne prise en charge des patients.
En 2022, la société italienne a développé un thermocycleur à faible encombrement, de la taille d’une souris d’ordinateur, décliné sous le terme de Molecular Mouse.
Les applications sont multiples pour aider les laboratoires à fournir aux patients les plus fragiles un diagnostic rapide d’identification bactérienne et de résistance à partir d’une hémoculture positive.
La Molecular Mouse est capable de détecter 44 agents pathogènes et 20 gènes de résistance en une heure sans extraction. Après une simple coloration de Gram, le laboratoire choisit parmi différents panels : GRAM POS STAPH et résistances, GRAM POS non STAPH et résistances, GRAM NEG ID qui couvre 96 % des bactéries généralement présentes, GRAM NEG RES complet (KPC, VIM, NDM, IMP, OXA-23 like, OXA-48 like, SHV, SHV ESBL, CTX-M group1/9, CTX-M group 2/8, CMY-2, mcr-1 et mcr-2). De nombreuses publications démontrent l’excellente corrélation de la méthode par puce RFID tag et l’apport dans la simplification du flux de travail.
EQUIPEMENT DE LABORATOIRE
Nouveau thrombo-agrégomètre

Stago propose une nouvelle version du thrombo-agrégomètre avec un panel complet d’agonistes validés et conformes aux recommandations internationales.
Utilisant la technologie « Gold Standard » de l’agrégation plaquettaire par transmission lumineuse, le TA8V permet une simplicité d’usage marquée par un gain de temps avec les 4 ou 8 puits, des tests standardisés, une traçabilité des réactifs et un historique patient ainsi qu’un enregistrement et une superposition des courbes en temps réel.
Les agonistes disponibles sont l’ADP, le collagène, l’épinéphrine, le TRAP-6 et l’acide arachidonique. Ils possèdent un conditionnement standardisé de 3 flacons d’1 mL lyophilisés à reconstituer avec 1 mL d’eau et une longue stabilité. Stago propose aussi de la ristocétine dans le cadre du test RIPA pour la caractérisation de la maladie de Von Willebrand.
INFORMATIQUE DE LABORATOIRE
Middleware amélioré pour la gestion bactériologique de pointe

Clarisys présentera lors du congrès de la RICAI les 14 et 15 décembre 2024 la mise à jour du middleware spécialisé Bac’Express, conçu pour offrir aux laboratoires une gestion bactériologique plus intuitive et performante. Avec une interface dédiée à la bactériologie, les biologistes bénéficient d’une validation simplifiée et d’outils spécialisés pour gérer efficacement leurs analyses.
Bac’Express, connu et éprouvé pour sa capacité à simplifier la gestion des antibiogrammes et des cultures bactériennes, intègre désormais de nouvelles fonctionnalités redessinées pour une expérience utilisateur plus ergonomique.
Cette version repensée offre une centralisation de l’antériorité d’identification des germes et des antibiogrammes. Pour une meilleure traçabilité et comparaison des résultats, jusqu’à 12 mois de demandes antérieures seront visualisables dans l’objectif de l’optimisation des traitements patients.
La v.9.2.0 de Bac’Express sera disponible dès janvier 2025. Clarisys sera sur le stand n°25 de la RICAÏ les 14 et 15 décembre 2024 au Palais de Congrès Porte Maillot à Paris.
INFORMATIQUE DE LABORATOIRE
Une nouvelle approche pour optimiser le contrôle qualité
LaboSmart-CQ, développé par Softech58, est un nouveau logiciel SaaS destiné aux laboratoires de biologie médicale. Il permet d’automatiser et de centraliser les contrôles qualité, tout en assurant la traçabilité des données et l’évaluation des performances du laboratoire, le tout via une interface intuitive et flexible.
Voici quelques-uns des nombreux avantages de LaboSmart-CQ :
1. Gain de temps : l’optimisation des saisies permet aux équipes de se concentrer sur des tâches à plus forte valeur ajoutée.
2. Automatisation des tâches CIQ/EEQ : la réduction des erreurs humaines et la libération du temps grâce à l’automatisation des processus de conformité et d’évaluation de la qualité.
3. Qualité et traçabilité : l’assurance d’une documentation précise et facilement traçable, garantissant la sécurité des données sensibles.
4. Suivi des performances : le bénéfice d’une amélioration continue grâce à un suivi constant des indicateurs de performance.
5. Rapports d’enquêtes automatiques : génération rapide des rapports pour faciliter la prise de décision.
MATERIEL DE LABORATOIRE
Gamme élargie pour le stockage des échantillons

Safe® Starter Pack Medium : Stockage des micro-tubes dans des boîtes au format SBS, avec lecteur de plaques et de tubes.

Plateau/portoir

Portoir 50 tubes

Solution pour boîtes SBS
AccsA’tech, expert dans la gestion et le stockage de sérothèques et de biobanques, a renforcé sa gamme Sero’Box® avec de nouvelles solutions innovantes, conçues pour optimiser la gestion et la traçabilité des échantillons biologiques. Grâce à une approche clé en main ou sur mesure, AccsA’tech propose trois nouvelles solutions pour répondre aux besoins variés des laboratoires et centres de recherche :
1. La solution sur grand plateau portoir : permet de stocker les tubes primaires, avec 1122 positions sur chaque plateau. Chaque tube est géolocalisé dans le logiciel
Sero’Box®.
2. La solution sur portoir 50 tubes : permet une intégration avec des automates, idéale pour les environnements automatisés. Cette solution permet de stocker 50 tubes. Chaque tube est géolocalisé sur les portoirs, qui peuvent s’adapter sur les automates pré analytiques.
3. La solution boîtes SBS et micro-tubes : offre un rangement compact et flexible pour les échantillons de petite taille. Elle permet de stocker 75 boîtes SBS de 96 micro-tubes. Chaque boîte est géolocalisée sur les 75 emplacements du plateau.
Sero’Box® se distingue par sa grande modularité, renforcée en 2024 par un partenariat avec LVL technologies GmbH, spécialiste des boîtes SBS, micro-tubes et scanners spécifiques. Ce partenariat permet à AccsA’tech d’élargir ses options de stockage tout en offrant une traçabilité optimisée grâce à des équipements de pointe.
La gamme Sero’Box® comprend également une large sélection d’accessoires pour s’adapter à tous les besoins de stockage, avec des nouveautés à découvrir tout au long de l’année.

Ziwig obtient le forfait innovation et déploie ses ailes


Le 21 octobre, Ziwig ouvrait les portes de son laboratoire Ziwig Lab, à Tercis-les-Bains près de Dax (Landes), pour une journée d’échanges enrichissants autour de l’innovation en matière de santé des femmes. Cette journée a été marquée par une étape majeure pour la société : la validation par la HAS du forfait innovation pour le test salivaire Endotest pour l’endométriose.
La ministre de la Santé et de l’Accès aux soins, Geneviève Darrieussecq, a chaleureusement salué cette innovation française lors de son discours diffusé sous forme de vidéo : « Le projet Ziwig incarne l’excellence française en matière d’innovation médicale… Vous êtes le symbole de notre volonté de développer des solutions de santé plus modernes, plus humaines et plus accessibles pour toutes les femmes », a-t-elle déclaré. Le forfait innovation permettra à de nombreuses femmes d’accéder à Ziwig Endotest en France.
L’événement a rassemblé de nombreux médecins, partenaires et associations – Endomind, BAMP, Endométriose et Douleurs Neuro, Draw your Fight, Vivre avec l’Endo, Talksaboutfanny – qui ont activement participé aux échanges. Ce fut l’occasion de partager les expériences de praticiens et de patientes et de souligner les enjeux auxquels sont confrontées les patientes lors d’une table ronde dédiée à la prise en charge concrète de la santé des femmes. Les autorités de santé était également au rendez-vous, avec la présence du Dr Darmaillacq, représentant de l’URPS Nouvelle-Aquitaine, et du Dr Elleboode, DG de l’ARS Nouvelle-Aquitaine.
Ziwig Care : vers une prise en charge globale
L’événement a aussi marqué le lancement officiel de Ziwig Care, un programme ambitieux qui vise à améliorer la prise en charge des patientes au-delà du diagnostic. « Nous ne nous arrêtons pas au diagnostic. Avec Ziwig Care, nous voulons offrir un accompagnement complet et personnalisé, reliant les centres experts aux structures de proximité », a déclaré Yahya El Mir, président et fondateur de Ziwig aux côtés du Dr Claire Théodore, gynécologue de la maison de santé de Tercis-les-Bains.
Ziwig Care repose sur une approche intégrative, associant médecine de proximité, soutien personnalisé et recherche clinique grâce à la plateforme digitale Ziwig Connect. Ce programme vise à fluidifier la coordination entre les patientes et les professionnels de santé, en s’appuyant sur une organisation agile et des partenariats locaux. « Notre objectif est de proposer des parcours de santé coordonnés, préventifs et connectés à la recherche, pour une prise en charge durable de l’endométriose », a ajouté Yahya El Mir.
Basée à Lyon, Ziwig est spécialisée dans la santé des femmes grâce à l’analyse des ARN par l’IA. L’entreprise déploie un laboratoire de R&D à l’ICM à Paris et un site de production industrielle à Tercis-les-Bains et une plateforme digitale.
Seegene et Werfen finalisent un accord de partenariat sur une initiative de partage de technologies

Le coréen Seegene, leader dans le domaine du diagnostic moléculaire par PCR, et l’espagnol Werfen, spécialiste mondial du diagnostic, ont finalisé un accord de partenariat pour le partage de technologies. L’accord décrit la création d’une nouvelle entité en Espagne, appelée Werfen-Seegene, d’ici le premier semestre 2025.
Cette initiative vise à partager les technologies de pointe de Seegene en matière de diagnostic et d’analyse de données, telles que la PCR syndromique en temps réel et un système automatisé de développement de produits. La technologie innovante de PCR syndromique en temps réel de Seegene permet la détection simultanée de 14 agents pathogènes maximum dans un seul tube de réaction, fournissant des données quantitatives pour chaque cible. Les entreprises partenaires travailleront avec des scientifiques et des spécialistes locaux pour développer des tests de diagnostic adaptés à leurs besoins régionaux pour diverses maladies humaines, animales et végétales.
Werfen-Seegene donnera la priorité au développement de diagnostics pour les maladies infectieuses, notamment les tests de résistance aux antimicrobiens et aux médicaments, les tests de charge virale, le suivi des patients transplantés d’organes, les infections sexuellement transmissibles (IST) et les maladies régionales émergentes. En s’appuyant sur la solide infrastructure et le réseau local de Werfen, la NewCo créera des produits adaptés aux besoins de santé de l’Espagne. L’Espagne, quatrième plus grand marché de DIV en Europe, servira de plaque tournante stratégique pour étendre l’initiative à travers l’Europe et le monde. En outre, Werfen-Seegene dirigera les efforts visant à obtenir l’approbation CE-IVDR pour les dispositifs médicaux de diagnostic in vitro, favorisant ainsi davantage l’expansion de ces innovations.
Le soutien au dépistage systématique du CMV pendant la grossesse discuté
L’infection congénitale à cytomégalovirus (cCMV) est une infection fœtale dont les conséquences peuvent induire des séquelles graves pour le futur enfant. Son dépistage en cours de grossesse fait actuellement l’objet de nombreux débats. Les femmes les plus vulnérables sont celles qui n’ont encore jamais été infectées par le cytomégalovirus (CMV) (50 % de la population des femmes de 15 à 45 ans) et qui feront une primo-infection, notamment celles ayant déjà un enfant : le plus souvent âgé de moins de 3 ans, fréquentant une collectivité et au contact duquel 10 % de ces mères sont susceptibles de s’infecter pour la première fois juste avant ou au début de leur nouvelle grossesse. Lorsqu’elles sont infectées pendant cette période, le taux de transmission de l’infection à l’embryon est de 30 %.
Environ quatre nouveau-nés sur 1 000 en France (soit environ 2 900 par an) sont donc infectés par le CMV pendant leur vie intra-utérine et, parmi eux, environ 18 % (environ 500 par an) développeront des séquelles à moyen et long terme : déficit de l’audition, troubles de l’équilibre, déficit moteur, retard mental, constituant la première cause de handicaps neurosensoriels congénitaux dans notre pays, en dehors des anomalies génétiques.
Or, le dépistage sérologique maternel précoce permet de diagnostiquer une primo-infection à CMV péri-conceptionnelle chez des mères auparavant séronégatives et d’instaurer rapidement un traitement antiviral de la mère pour réduire la charge virale fœtale. Des données récentes démontrent l’efficacité d’un traitement précoce par Valaciclovir® à réduire de 70 % le risque de transmission virale d’infections fœtales et donc le risque de formes graves handicapantes. Ces résultats ont conduit un groupe européen à se positionner en faveur du dépistage systématique du CMV en début de grossesse, et l’Italie a d’ailleurs récemment mis en œuvre ces recommandations.
En France, un tel dépistage pourrait être organisé : les techniques sérologiques commerciales, disponibles et utilisées en routine, sont standardisées, automatisées et accessibles sur l’ensemble du territoire. Les réseaux de biologistes et de gynéco-obstétriciens, et les centres de référence du CMV sont à même de s’organiser pour élargir et soutenir l’implantation du dépistage du CMV, déjà en partie en place dans certaines régions, notamment l’Ile de France.
Un avis récent du Haut Conseil de la Santé Publique, écartant le dépistage précoce systématique de l’infection à CMV en début de grossesse, omet en particulier d’inclure, dans l’analyse des coûts induits pour la Société, la prise en charge à vie des enfants handicapés.
Selon la disposition légale par laquelle « l’État peut mettre en place, après avis de la Haute Autorité de santé (HAS), un programme de dépistage de cytomégalovirus (CMV) de façon systématique chez la femme enceinte », le Ministère de la santé vient de solliciter la HAS pour qu’elle rende son avis.
Académie Nationale de Médecine
La biologiste Edith Heard reçoit la médaille d’or 2024 du CNRS

© Frédérique PLAS / CNRS Images
La médaille d’or du CNRS, l’une des plus prestigieuses récompenses scientifiques françaises, est décernée cette année à la biologiste Edith Heard. Cette spécialiste mondiale de l’épigénétique est récompensée pour ses contributions exceptionnelles à l’avancement de sa discipline. Ses recherches, notamment sur l’inactivation du chromosome X, ouvrent de nouvelles perspectives tant en biologie qu’en médecine. Cette médaille, accompagnée d’une dotation de 50 000 euros de la Fondation CNRS, lui sera remise le 12 décembre 2024 lors d’une cérémonie à Paris.
Aujourd’hui directrice générale du Laboratoire européen de biologie moléculaire (EMBL) et professeure au Collège de France, Edith Heard est mondialement reconnue pour ses travaux pionniers sur l’inactivation du chromosome X, un processus essentiel au développement des embryons femelles. Ses recherches ont permis de dévoiler des mécanismes épigénétiques régulant l’expression des gènes, offrant une nouvelle compréhension des premiers stades embryonnaires ainsi que de la biologie des femmes. Ses découvertes ont révolutionné notre compréhension de l’épigénétique, discipline qui explore les changements dans l’activité des gènes qui définissent l’identité d’une cellule.
Antoine Petit, PDG du CNRS, a salué les réalisations de la lauréate : « Figure européenne et internationale éminente en épigénétique, Edith Heard est une référence de la biologie moderne comme en témoignent les nombreuses découvertes qui ont jalonné sa carrière et son engagement pour une recherche d’excellence. En lui décernant la médaille d’or 2024, le CNRS rend hommage à une biologiste à la carrière scientifique internationale d’exception et aussi à une biologiste mobilisée dans la promotion de la science et la formation des futurs leaders du domaine ».
Née en 1965 à Londres, Edith Heard a étudié les sciences naturelles à l’université de Cambridge, avant de s’intéresser à l’épigénétique lors de sa thèse sur l’amplification génique dans le cancer à la Fondation impériale de recherche contre le cancer (ICRF), à Londres. Elle arrive en France en 1990 grâce à une bourse d’étude du Human Frontier Science Program et rejoint l’Institut Pasteur pour un post-doctorat, puis le CNRS 3 ans plus tard.
Test POC de l’infection articulaire périprothétique en cinq minutes
© 123RF
L’infection articulaire périprothétique (IAP) représente un problème mondial important qui s’aggrave à mesure que le nombre de remplacements articulaires augmente en raison du vieillissement de la population. Rien qu’aux États-Unis, le nombre prévu d’arthroplasties de la hanche et du genou devrait quadrupler au cours des 10 à 20 prochaines années. L’IAP touche plus de 2 % de ces patients et est devenue la principale cause de révision d’arthroplastie. Un diagnostic rapide et précis de l’IAP est essentiel pour garantir que les patients reçoivent le plan de traitement chirurgical ou antimicrobien le plus adapté. Un test de pointe et de haute précision au point d’intervention est actuellement en cours de développement pour diagnostiquer l’IAP en moins de cinq minutes.
La société InfectoTest GmbH (Berlin, Allemagne) développe InfectoSynovia, un test rapide et de haute précision conçu pour identifier l’IPJ en moins de cinq minutes. Ce test utilise une technique d’analyse électrochimique innovante qui ne nécessite qu’un échantillon minimal de liquide synovial. Ce test pourrait réduire considérablement le temps de diagnostic à moins de cinq minutes tout en offrant une excellente sensibilité et spécificité, en utilisant un échantillon de 50 microlitres de liquide synovial seulement.
Grâce à l’approche d’analyse électrochimique unique de la société, complétée par un logiciel qui aide à l’interprétation précise des résultats, ce test sera capable de détecter les infections de bas grade et les infections à culture négative. Cette technologie révolutionnaire vise à transformer le diagnostic de l’IPJ, répondant à une demande mondiale croissante alors que la prévalence des remplacements articulaires augmente avec le vieillissement de la population.
Vers une caractérisation rapide des bactéries résistantes
Une approche diagnostique innovante pour les infections bactériennes pour permettre un traitement plus rapide et efficace.
Les méthodes actuelles de cultures bactériennes prennent plusieurs jours pendant lesquels les patients se voient souvent prescrire des antibiotiques à large spectre, qui peuvent créer des infections résistantes aux médicaments, ce qui constitue un problème de santé publique majeur. Aujourd’hui, une approche diagnostique innovante pourrait potentiellement permettre aux patients atteints d’infections bactériennes de recevoir le traitement le plus efficace plus rapidement.
La méthode, baptisée test de sensibilité génotypique et phénotypique aux antibiotiques par détection d’ARN, ou GoPhAST-R, a été développée par des chercheurs du Broad Institute du MIT et de Harvard, en collaboration avec le Massachusetts General Hospital (Cambridge, MA, États-Unis). Cette technique analyse à la fois la croissance et l’activité génétique des bactéries pour évaluer rapidement la sensibilité de l’agent pathogène à divers antibiotiques. Dans l’approche GoPhAST-R, des échantillons bactériens sont exposés à une gamme d’antibiotiques, après quoi une plateforme de détection d’ARN est utilisée pour identifier des modèles distincts de changement dans l’expression de l’ARN messager, qui indiquent des différences dans l’activité des gènes bactériens. Ces changements d’ARNm se produisent dans les minutes qui suivent l’exposition aux antibiotiques chez les bactéries sensibles aux médicaments, alors qu’ils n’apparaissent pas chez les souches résistantes aux médicaments. En outre, la méthode étudie les gènes associés à la résistance aux antibiotiques, pour mieux comprendre les mécanismes bactériens sous-jacents et suggérer des options thérapeutiques potentielles. Les chercheurs ont également démontré l’efficacité de l’approche dans une étude pilote portant sur des hémocultures de patients recevant un traitement hospitalier pour des infections.
Dans leur travail précédent avec un nombre limité d’échantillons de patients, l’équipe de recherche a démontré que GoPhAST-R pouvait déterminer la sensibilité aux antibiotiques en moins de quatre heures après la détection des bactéries dans une hémoculture. Dans la nouvelle étude, ils ont élargi le pilote clinique pour inclure des échantillons de sang de 42 patients hospitalisés pour des infections causées par E. coli ou Klebsiella pneumoniae, soit les agents pathogènes les plus courants responsables d’infections sanguines. Les chercheurs ont exposé les hémocultures à 9 antibiotiques différents de 3 classes distinctes et ont ensuite effectué un profilage transcriptionnel sur la plateforme NanoString. Ils ont analysé les changements d’ARNm dans 10 gènes pour chaque classe d’antibiotiques, ainsi que quelques gènes sélectionnés qui confèrent une résistance aux antibiotiques bêta-lactamines. Leurs résultats ont démontré une concordance de 95 % avec ceux obtenus à partir d’essais de référence basés sur la croissance pour la sensibilité aux antibiotiques.
MANIFESTATIONS
2024
– 16-17 décembre – 44e Réunion Interdisciplinaire de Chimiothérapie Anti-Infectieuse – RICAI – PARIS – www.ricai.fr/
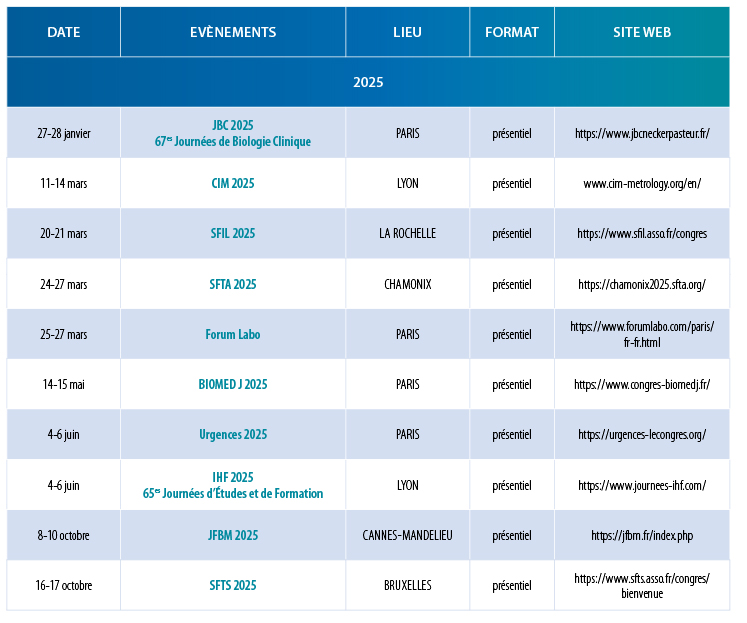
2025
– 27-28 janvier – JBC 2025 – 67es Journées de Biologie Clinique – PARIS – https://www.jbcneckerpasteur.fr/
– 11-14 mars – CIM 2025 – LYON – https://www.cim-metrology.org/en/press
– 20-21 mars – SFIL 2025 – LA ROCHELLE – https://www.sfil.asso.fr/congres
– 24-27 mars – SFTA 2025 – CHAMONIX – https://chamonix2025.sfta.org/
– 25-27 mars – Forum Labo – PARIS – https://www.forumlabo.com/paris/fr-fr.html
– 14-15 mai – BIOMED J 2025 – PARIS – https://www.congres-biomedj.fr/
– 4-6 juin – Urgences 2025 – PARIS – https://urgences-lecongres.org/
– 4-6 juin – IHF 2025 – 65es Journées d’Études et de Formation – LYON – https://www.journees-ihf.com/
– 3-10 octobre – JFBM 2025 – CANNES-MANDELIEU – https://jfbm.fr/index.php
– 16-17 octobre – SFTS 2025 – BRUXELLES – https://www.sfts.asso.fr/congres/bienvenue
Screenshot
Retrouvez dans Spectra Diagnostic N°35 :
BOURSE & BIOTECHS
L’après-Covid de Pfizer : le désenchantement
Arsia AMIR-ASLANI, Phoung Duy TO, Aidan PRICE, Georges EL HADDAD
TECHNOLOGIE APPLIQUÉE
L’Architecture Zero Trust dans le développement de middleware au sein des laboratoires : une analyse approfondie
Lisa VONSTEIN
CAS BIOCLINIQUES
Recommandations sur les explorations biologiques nécessaires dans les cas particuliers de dermato-immunologie
Chloé BOST, Caroline CARLE, Françoise FORTENFANT
CAS BIOCLINIQUES
Anticorps anti-MPO : diluer, est-ce une bonne idée ?
Stéphanie ROGEAU, Mathieu TRONCHON, Aurore COLLET, Anne-Sophie DELEPLANCQUE, Sylvain DUBUCQUOI
CAS BIOCLINIQUES
Dermatomyosite juvénile : importance du bilan auto-immun
Daniela LAKOMY, Justine COSME
CAS BIOCLINIQUES
Un cas de pemphigoïde de la grossesse
Thibaut BELMONDO
TECHNOLOGIE APPLIQUÉE
Synoptique : Les Middlewares en 2024






